Вопросы вирусологии
Международный рецензируемый научно-практический журнал «Вопросы вирусологии» (транслитерированное основное название «Voprosy virusologii», параллельное название - Problems of Virology, ISSN (Print) 0507-4088, ISSN (Online) 2411-2097) знакомит читателей с достижениями российской и мировой вирусологии, размещает на своих страницах статьи, посвященные изучению вирусов и вирусных болезней человека, животных и растений.
Видное место в журнале отводится публикации результатов экспериментальных работ по различным вопросам общей и частной вирусологии.
Журнал публикует материалы, способствующие внедрению в практику достижений вирусологической науки по ликвидации и снижению распространенности инфекционных заболеваний, а также их диагностике, профилактике и лечению.
В обзорных статьях обобщаются последние достижения в области вирусологии. С целью привлечения внимания вирусологов к наиболее актуальным вопросам, требующим дальнейшего изучения, в журнале публикуются редакционные заметки и рецензии на книги. Читатель найдет в журнале описание новых методов исследований, методических приемов, новой аппаратуры, средств диагностики и лечения.
Журнал рассчитан на вирусологов (медиков и ветеринаров), эпидемиологов, паразитологов, фармакологов, биохимиков и других специалистов.
«Вопросы вирусологии» - журнал открытого доступа, не берущий плату за публикацию научных статей.
Журнал входит в SCOPUS (Q4).
В соответствии с рекомендациями ВАК (Письмо ВАК от 06.12.2022 № 02-1198), журнал относится к категории К1 как издание, входящее в базы данных SCOPUS и RSCI.
Журнал, входит в рекомендованный ВАК «Перечень рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук, на соискание ученой степени доктора наук» (в соответствии с п.5 Правил формирования Перечня (Приказ Минобрнауки России от 12.12.2016 N 1586), как входящий в международную реферативную базу данных и систем цитирования Scopus) по специальностям:
- 1.5.10. Вирусология (медицинские и биологические науки)
- 3.2.2. Эпидемиология (медицинские и биологические науки)
- 3.1.22. Инфекционные болезни (медицинские и биологические науки)
- 3.3.6 Фармакология, клиническая фармакология (медицинские и биологические науки)
Журнал представлен в следующих международных базах библиографических данных и информационно-справочных системах: РИНЦ, RSCI (на платформе WoS), Abstract Journals, AIDS & Cancer Research, Biocontrol News and Information, Biological Sciences, Chemical Abstracts, DOAJ, EBSCOhost Biological Abstracts, EBSCOhost Wildlife & Ecology Studies Worldwide, Elsevier BV Scopus, Elsevier BV EMBASE, Index Medicus, Excerpta Medica, Index Veterinarius, MEDLINE, National Library of Medicine PubMed, Parasitology Database, Poultry Abstracts, Review of Medical and Veterinary Entomology, SCOPUS, Thomson Reuters Biological Abstracts, Thomson Reuters BIOSIS Previews, Thomson Reuters Science Citation Index Expanded, Thomson Reuters Web of Science, Tropical Diseases Bulletin, Veterinary Science Database, Virology and AIDS Abstracts, ROAD.
В 2022 г журнал вошел в DOAJ и удостоен DOAJ SEAL.
Контент доступен под лицензией Creative Commons — Attribution 4.0 International, CC-BY.
Каждой статье журнала присваивается идентификатор цифрового объекта — DOI.
Все публикуемые в журнале статьи, обзоры и лекции проходят обязательное двойное слепое рецензирование членами редколлегии и приглашенными экспертами.
Статьи иностранных авторов, а также русскоязычные статьи, отдельно рекомендованные редколлегией, публикуются на русском и английском языке под единым DOI. Перевод носителем языка и научное редактирование перевода производится за счет Редакции.
Журнал выходит 1 раз в 2 месяца (6 выпусков в год).
Журнал является органом Общероссийской общественной организации «Всероссийское научно- практическое общество эпидемиологов, микробиологов и паразитологов».
Учредители:
- ФБУН ЦНИИ Эпидемиологии Роспотребнадзора,
- Общероссийская общественная организация «Всероссийское научно-практическое общество эпидемиологов, микробиологов и паразитологов».
Издатель:
- ФБУН ЦНИИ Эпидемиологии Роспотребнадзора.
При регистрации на сайте читатели и авторы получают автоматические уведомления о содержании новых выпусков Журнала на адрес своей электронной почты с возможностью отписаться от рассылки.
Текущий выпуск
Том 69, № 2 (2024)
РЕДАКЦИОННАЯ КОНЦЕПЦИЯ
Птичий грипп: «по ком звонит колокол»?
Аннотация
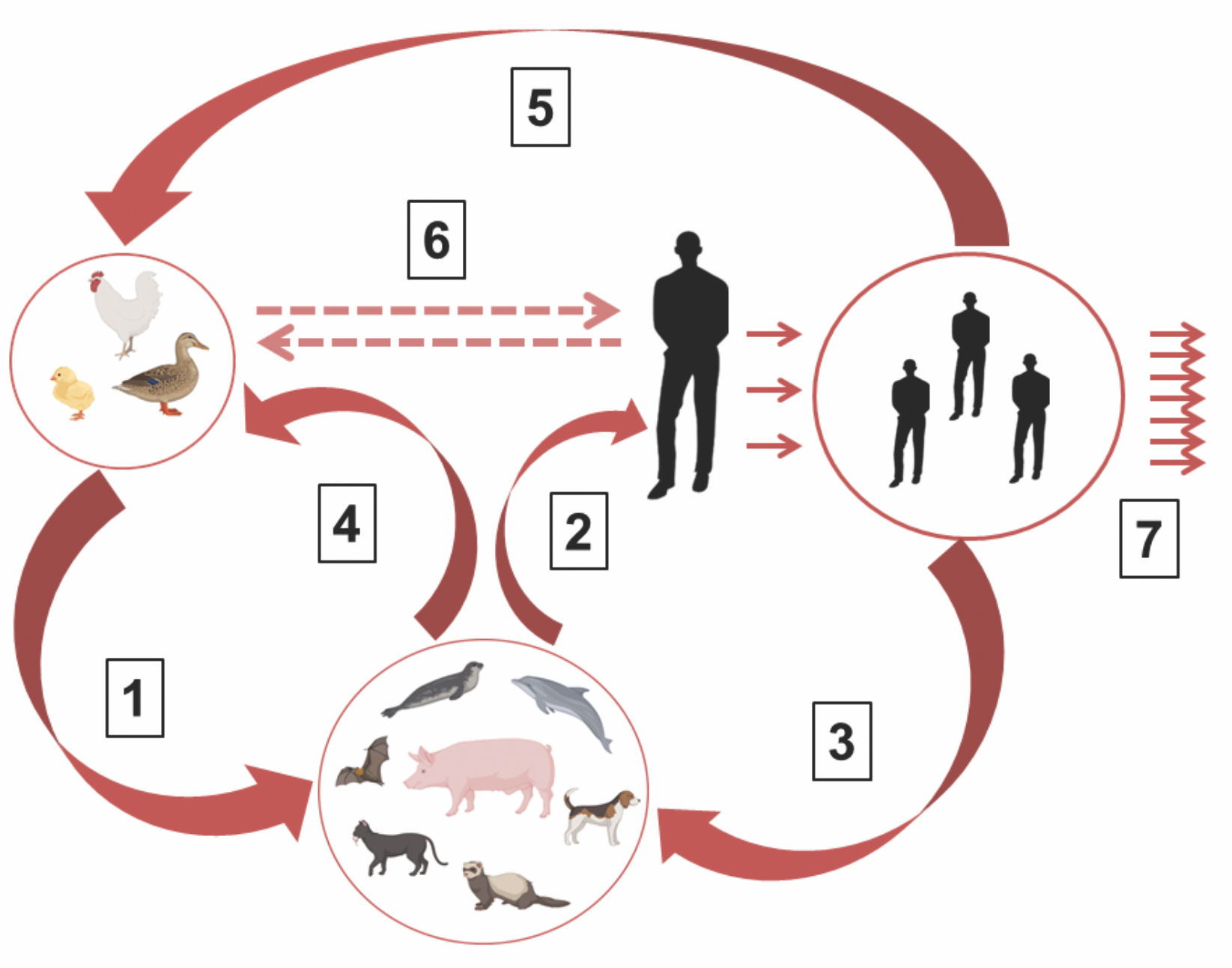
Семейство Orthomyxoviridae состоит из 9 родов, включая Alphainfluenza viruses, куда входят вирусы гриппа птиц. У двух субтипов ‒ Н5 и Н7 ‒ помимо обычных низковирулентных штаммов описана особая разновидность высоковирулентного вируса птиц, способного вызывать заболеваемость у птиц с летальностью выше 60%. Эти и ряд других разновидностей вируса гриппа, тесно связанных с птицами, принято обозначать термином «птичий вирус гриппа». Различие высоко- (HPAI) и низковирулентных (LPAI) вирусов гриппа обусловлено структурой аргининсодержащего сайта протеолитической активации в белке НА. Вирус высоковирулентного птичьего гриппа Н5 выявлен около 100 лет назад и на протяжении этого времени вызывает эпизоотии среди диких и домашних птиц, и лишь несколько локальных эпизодов болезни зарегистрированы среди людей с начала XXI в. В последние годы зафиксирован резкий подъем заболеваемости птиц высоковирулентным вирусом Н5N1 (клайд h2.3.4.4b) на всех континентах планеты, сопровождающийся переходом вируса на разные виды млекопитающих. Регистрируемая глобальная смертность среди домашних и сельскохозяйственных птиц от данного субтипа приближается к уровню 1 млрд особей. Опасным эпидемическим фактором становятся участившиеся вспышки птичьего гриппа с высокой летальностью среди млекопитающих, в частности морских львов и тюленей в Северной и Южной Америке, норок и пушных зверей в Испании и Финляндии, домашних и уличных кошек в Польше. Изолированные от млекопитающих штаммы птичьего гриппа H5N1 клайда h2.3.4.4b имеют признаки частичной адаптации к организму человека в генах РВ2, NP, HA, NA, играющих главную роль в регуляции аэрозольной трансмиссии и круга хозяев вируса. Создавшаяся ситуация представляет реальную угрозу предадаптации вируса в организме млекопитающих как промежуточных хозяев с последующим переходом предадаптированного вируса в популяцию людей и формированием пандемии с катастрофическими последствиями.
 101-118
101-118


ОБЗОРЫ
Применение иммуноглобулинов и моноклональных антител в отношении COVID-19
Аннотация
Введение. При возникновении нового заболевания одним из наиболее доступных средств с установленной и доказанной терапевтической эффективностью в первую очередь являются препараты, содержащие специфические антитела к данному инфекционному агенту. Введение таких препаратов направлено на снижение количества возбудителя в макроорганизме и, как следствие, уменьшение тяжести симптомов заболевания либо выздоровление.
Целью настоящего обзора является анализ опыта использования иммуноглобулинов и моноклональных антител при лечении больных COVID-19 в ходе пандемии.
Результаты и заключение. Двумя основными группами медицинских средств защиты, блокирующих проникновение вируса SARS-CoV-2 в пермиссивные клетки, являются препараты, получаемые из плазмы крови реконвалесцентов (иммуноглобулин), и человеческие моноклональные антитела. В первой группе препаратов при лечении больных COVID-19 ведущее место занимает плазма крови реконвалесцентов. Данный препарат с успехом может быть использован для проведения экстренной профилактики на ранних стадиях заболевания. Основным недостатком терапии при использовании плазмы крови реконвалесцентов является трудность стандартизации ввиду значительного варьирования содержания специфических антител у доноров. Другим недостатком терапии при использовании препаратов первой группы являются нежелательные побочные реакции у реципиентов, возникающие при их введении. Альтернативным подходом при проведении терапии COVID-19 является использование гуманизированных и генно-инженерных человеческих моноклональных антител против определенных эпитопов вируса SARS-CoV-2, в частности, рецептор-связывающего домена S-белка, способных предотвратить проникновение вируса в пермиссивные клетки и прервать развитие манифестной инфекции. Преимуществами данных препаратов является их безопасность, высокая специфическая активность, возможность стандартизации, однако сложность их производства и высокая стоимость делают их малодоступными для массового использования в практической медицине.
 119-126
119-126


ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Профилирование экспрессии генов p53 и c-myc у HTLV-1-инфицированных доноров крови в Конго
Аннотация
Введение. Инфекция HTLV-1 сохраняется в течение всей жизни человека, обусловливая бессимптомное вирусное носительство у большинства пациентов и обеспечивая цепь передачи. Однако примерно у 4% инфицированных развивается Т-клеточная лейкемия/лимфома взрослых (ATLL). HTLV-1 – это онкоретровирус, который трансформирует CD4+-Т-лимфоциты и дерегулирует лимфопролиферативные пути, что способствует развитию ATLL. Для достижения трансформации клеток большинство онкогенных ретровирусов используют трансдукцию с захватом протоонкогенов, при этом провирусная интеграция нарушает экспрессию опухолевых супрессоров или протоонкогенов.
Цель исследования. Мы провели исследование по определению распространенности HTLV-1-инфекции среди доноров крови с целью расширения базы данных HTLV-1, оценки риска передачи вируса через компоненты крови, а также оценки риска персистенции инфекции или развития неопластических заболеваний у носителей HTLV-1.
Материалы и методы. Настоящая научная работа – перекрестное исследование доноров крови всех категорий. В исследовании участвовали 265 доноров крови из Национального центра переливания крови в Браззавиле. После тестирования на антитела к HTLV-1 методом ИФА во всех положительных в ИФА-образцах проводили определение провирусной ДНК методом «вложенной» ПЦР, а затем методом количественной ОТ-ПЦР с использованием специфических праймеров p53 и c-myc оценивали экспрессию генов.
Результаты. Из 265 доноров 20 человек были положительны по анти-HTLV-1-антителам, у 5 доноров была выявлена провирусная ДНК. Распространенность HTLV-1 составила 1,8%. Все HTLV-1-инфицированные доноры были мужчинами (1,8%), с положительной корреляцией между наличием инфекции и мужским полом (p = 0,05); 1,1% положительных доноров были регулярными, большинство в возрасте от 31 до 45 лет (1,5%), и наиболее часто встречались доноры-совместители (1,1%). Во всех образцах наблюдалась нормальная экспрессия генов p53 и c-myc.
Заключение. Распространенность HTLV-1, хотя и низкая, остается значительной проблемой. У HTLV-1-инфицированных доноров не было обнаружено аномальной экспрессии генов p53 или c-myc, что может означать, что ни один из Т-лимфоцитов доноров не был трансформирован HTLV-1.
 127-133
127-133


Обнаружение и высокое содержание ДНК герпесвирусов (Orthoherpesviridae) в аутопсийных материалах пациентов с летальным исходом COVID-19
Аннотация
Введение. Вирус SARS-CoV-2 вызывает нарушения иммунитета, создающие условия для реактивации герпесвирусов человека (ГВЧ). Однако влияние ГВЧ на течение и исход COVID-19 оценивается неоднозначно.
Цель исследования – изучение возможной связи между реактивацией ГВЧ у пациентов, инфицированных SARS-CoV-2, и неблагоприятным исходом COVID-19.
Материалы и методы. Посмертные клинические материалы из головного мозга, печени, селезенки, лимфоузлов и легких были получены от 59 пациентов, находившихся на лечении в ГБУЗ ИКБ № 1 ДЗ г. Москвы в 2021–2023 гг. В 1-ю группу включили материалы от 39 пациентов с летальным исходом COVID-19; во 2-ю группу – от 20 пациентов, не инфицированных SARS-CoV-2 и умерших от разных соматических заболеваний. ДНК ГВЧ и РНК SARS-CoV-2 определяли методом ПЦР.
Результаты. В аутопсийных образцах ДНК ГВЧ была обнаружена у всех пациентов в обеих группах. В 1-й группе вирус Эпштейна‒Барр (ВЭБ) чаще обнаруживали в лимфоузлах (94%), вирус герпеса человека 6-го типа (ВГЧ-6) – в печени (68%), цитомегаловирус (ЦМВ) – в лимфоузлах (18%), вирус простого герпеса (ВПГ) – в головном мозге (16%), вирус варицелла-зостер (ВЗВ)– в легких и селезенке (по 3%). Различия в частоте встречаемости ГВЧ между группами были статистически незначимыми. Важные различия установлены при анализе вирусной нагрузки. У 1-й группы количество проб, содержавших более 1000 копий ДНК ГВЧ на 100 тыс. клеток, составляло 52,4%, во 2-й группе – 16,6% (p < 0,002). Установлена ассоциация между реактивацией ВПГ и ВГЧ-6 и тяжестью поражения легких. Активация ВЭБ коррелировала с повышением уровней ферментов печени.
Заключение. Полученные результаты свидетельствует о реактивации ГВЧ у пациентов с летальным исходом COVID-19. Обнаружение ГВЧ ассоциировалось с тяжелыми повреждениями легких и печени, что указывает на связь реактивации ГВЧ со смертельными исходами COVID-19.
 134-150
134-150


Встречаемость и генетическое разнообразие вируса Алонгшан (Flaviviridae), выявленного в клещах на юге Восточной Сибири
Аннотация
Введение. Инфекции, переносимые иксодовыми клещами, являются значимой проблемой для многих регионов России, в том числе и для Восточной Сибири. Неблагополучная эпидемиологическая ситуация может характеризоваться не только ростом встречаемости уже известных «клещевых» инфекций, но и выявлением новых нозологических форм и возбудителей, роль которых остается малоизученной или вообще неизученной. Сегментированные флавиподобные вирусы могут быть причиной инфекционных заболеваний человека и создавать угрозу для здоровья населения.
Цель работы ‒ поиск и молекулярно-генетическая характеристика изолятов вируса Алонгшан (Flaviviridae: Alongshan virus, ALSV), переносимого клещами на юге Восточной Сибири.
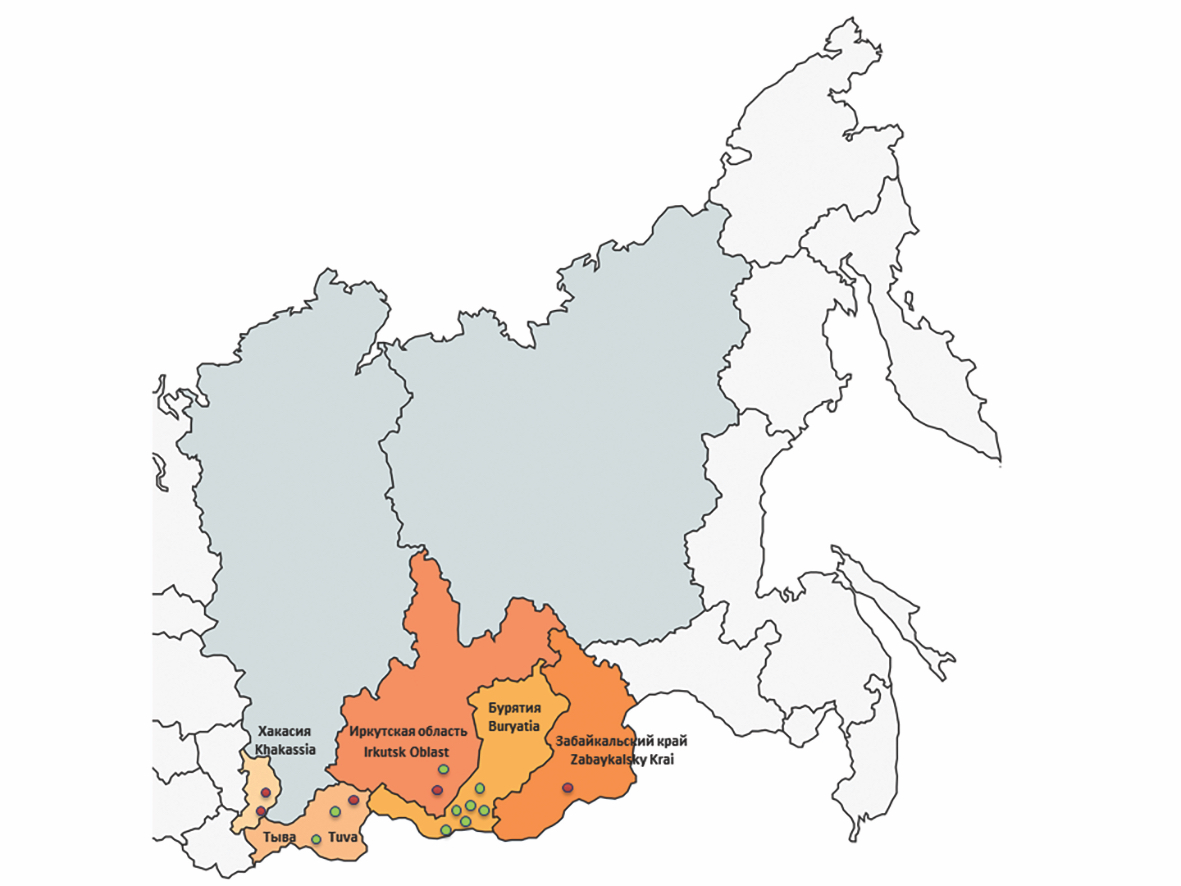
Материалы и методы. Было собрано и исследовано 1060 клещей, отловленных на территории Республик Хакасия, Тыва, Бурятия, Иркутской области и Забайкальского краяв весенне-летний период 2023 г. Детекцию РНК ALSV выполняли с помощью метода полимеразной цепной реакции с обратной транскрипцией с последующим определением нуклеотидной последовательности и проведением филогенетического анализа для каждого из 4 сегментов генома.
Результаты. Инфицированность ALSV клещей Ixodes persulcatus, собранных в Республике Хакасия, составила 3,3% (95% ДИ 1,4–7,5), в Иркутской области – 1% (95% ДИ 0,3–3,7), в Республике Тыва – 0,9% (95% ДИ 0,3–3,4), в Забайкальском крае – 0,7% (95% ДИ 0,2–3,6). Генетические варианты ALSV, циркулирующие в клещах I. persulcatus на территории юга Восточной Сибири, по всем 4 сегментам группируются с последовательностями, обнаруженными в Китае, и кластеризуются в азиатскую подгруппу, переносимую таежным клещом. Уровень различия нуклеотидных последовательностей фрагментов генома среди выявленных генетических вариантов ALSV составил от 2 до 3%.
Заключение. Показано широкое распространение ALSV в клещах I. persulcatus на территории республик Хакасия и Тыва, Иркутской области и Забайкальского края. Эти данные актуализируют мониторинг за изменением ареала распространения флавиподобных вирусов, потенциально опасных для человека, и их переносчиков.
 151-161
151-161


Филогенетический анализ вариантов вируса Пуумала (Hantaviridae: Orthohantavirus), циркулирующих на территории Саратовской области
Аннотация
Цель работы – определение полной нуклеотидной последовательности и проведение филогенетического анализа вариантов геномов вируса Пуумала, выделенных на территории Саратовской области.
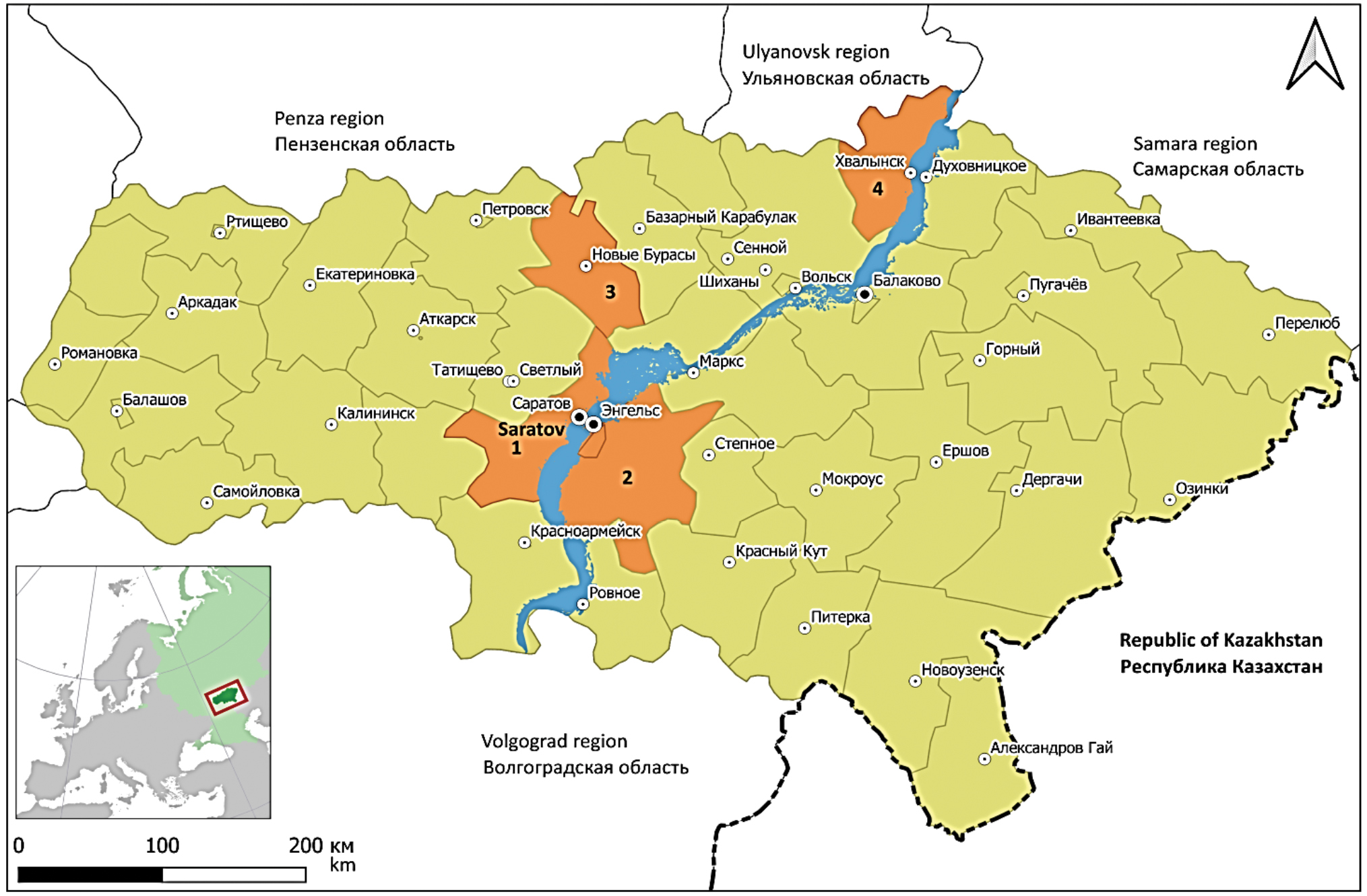
Материалы и методы. Образцами для исследования послужил полевой материал, собранный в Гагаринском (бывшем Саратовском), Энгельсском, Новобурасском и Хвалынском районах Саратовской области в период с 2019 по 2022 г. Для специфического обогащения генома вируса Пуумала в образцах использовали ПЦР и панель праймеров, подготовленную для данного исследования. Далее проводили секвенирование полученных продуктов реакции и сборку фрагментов в одну последовательность для каждого из сегментов генома вируса. При построении филогенетических деревьев применяли алгоритм maximum parsimony.
Результаты. Показано, что генетические варианты вируса Пуумала, выделенные в Саратовской области, имеют высокую степень подобия генома, что говорит о единстве их происхождения. По данным филогенетического анализа, все выделенные варианты вируса (за исключением изолятов вируса из Хвалынского района) образуют обособленную ветвь в кластере, сформированном хантавирусами из других субъектов Приволжского федерального округа. Самыми близкими к образцам из Саратовской области являются варианты вируса из республик Удмуртия и Татарстан, а также из Самарской и Ульяновской областей.
Заключение. Полученные данные указывают на наличие выраженной территориальной приуроченности штаммов к определенным регионам или областям, являющимся природными биотопами их носителей. Этот факт позволяет довольно точно определять территорию возможного инфицирования заболевших и/или циркуляцию переносчиков данных вариантов вируса по последовательности отдельных сегментов их генома.
 162-174
162-174


Разработка, получение и характеристика вирусоподобных частиц SARS-CoV-2 (Coronaviridae: Orthocoronavirinae: Betacoronavirus: Sarbecovirus)
Аннотация
Введение. Пандемия COVID-19, вызванная коронавирусом SARS-CoV-2, породила серьезные проблемы в здравоохранении по всему миру. Ученым в кратчайшие сроки пришлось решать задачи по разработке методов лечения и профилактики этого заболевания. Наиболее эффективным способом прерывания развивающихся новых эпидемических вспышек является вакцинация. Одним из современных и эффективных подходов при разработке вакцин является использование вирусоподобных частиц (Virus like particles, VLP).
Цель исследования – разработать технологию получения VLP на основе рекомбинантных белков SARS-CoV-2 (E, M, N и S), продуцируемых в клетках насекомых, и дать их комплексную характеристику.
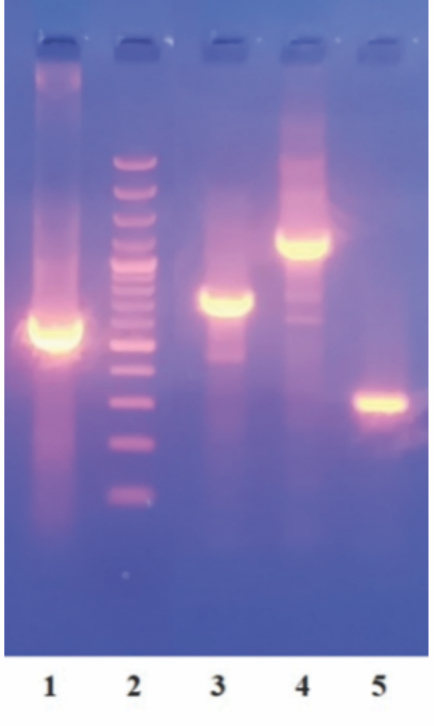
Материалы и методы. Источником вирусных белков послужили синтетические гены, кодирующие белки коронавируса E, M, N и S. Были разработаны VLP с разными поверхностными S-белками 4 штаммов коронавируса: подобный вирусу Ухань, Delta, Alpha и Omicron, клонированные в плазмиду pFastBac. Белки были синтезированы в бакуловирусной системе экспрессии и собраны в VLP в перевиваемой линии клеток Trichoplusia ni (T.ni). Синтез генов, клонирование в трансферные плазмиды и получение рекомбинантных бакуловирусов проводили стандартными методами. Наличие вставки в геноме бакуловируса определяли методом полимеразной цепной реакции. Для исследования антигенной активности VLP применяли иммуноферментный анализ, иммуноблоттинг. Очистку VLP проводили ультрацентрифугированием через 20% сахарозу. Оценку морфологии выполняли с помощью электронной микроскопии и методом динамического светорассеяния.
Результаты. Получены и охарактеризованы VLP, состоящие из рекомбинантных белков S, M, E и N, на основе консенсусных последовательностей, циркулирующих в мире геновариантов SARS-CoV-2. Показана специфичность антигенных детерминант синтезированных VLP антителам, формирующимся к белкам SARS-CoV-2, изучены иммуногенные свойства VLP.
Заключение. Разработаны способы получения и очистки VLP с универсальным набором поверхностных антигенов, способных к самосборке и индуцирующих специфический иммунитет против SARS-CoV-2.
 175-186
175-186


КРАТКИЕ СООБЩЕНИЯ
Серопревалентность вируса простого герпеса 1-го типа (Herpesviridae: Simplexvirus: Human alphaherpesvirus 1) у курильщиков
Аннотация
Введение. Вирус простого герпеса 1-го типа (ВПГ-1) – один из самых распространенных вирусных агентов, инфицирующих человека, имеет геном с двухцепочечной ДНК и относится к семейству Herpesviridae. Курение – одна из основных причин заболеваний и преждевременной смерти во всем мире, от которой ежегодно умирает до 6 млн человек.
Цель настоящего исследования – определение серопревалентности ВПГ-1 среди курильщиков.
Методы. Исследование проводили в период с декабря 2022 г. по январь 2023 г. В исследование была включена случайная выборка из 94 (88 мужчин и 6 женщин) здоровых лиц в возрасте от 20 до 60 лет, 50 участников составили контрольную группу. Серологическое тестирование на ВПГ заключалось в выявлении антител к ВПГ-1 класса IgG с помощью ИФА.
Результаты. Большинство участников были студентами университета – 45,7% мужчин и 5,3% женщин, за ними следовали работающие курильщики – 0,2% мужчин и 1,1% женщин. Число женщин было значительно меньше, чем мужчин, и составило 6,4 и 93,6% соответственно, что объясняется обычаями и традициями. Серопревалентность составила 24,47, 22,3 и 2,1% среди мужчин и женщин соответственно. Уровень серопревалентности составил 13,8% среди курильщиков кальяна и сигарет, 9% исключительно среди курильщиков сигарет и 1,1% исключительно среди курильщиков кальяна. Наибольший уровень выявляемости антител наблюдался в возрастных группах 21–30 и 31–40 лет – 12,80 и 7,40% соответственно.
Заключение. Исследование показало, что серопревалентность ВПГ-1 IgG составила 24,47% и была выше среди курильщиков кальяна и сигарет по сравнению с теми, кто курил исключительно сигареты или кальян.
 187-192
187-192


ЮБИЛЕЙНЫЕ ДАТЫ
 193-194
193-194