Comparative study of Wuhan-like and omicron-like variants of SARS-CoV-2 in experimental animal models
- Authors: Leneva I.A.1, Smirnova D.I.1, Kartashova N.P.1, Gracheva A.V.1, Ivanina A.V.1, Glubokova E.A.1, Korchevaya E.R.1, Pancratov A.A.2, Trunova G.V.2, Khokhlova V.A.2, Svitich O.A.1, Zverev V.V.1, Faizuloev E.B.1
-
Affiliations:
- Mechnikov Research Institute of Vaccines and Sera, Department of Virology
- Herzen Moscow Research Institute of Oncology of the Ministry of Health of Russia
- Issue: Vol 67, No 5 (2022)
- Pages: 439-449
- Section: ORIGINAL RESEARCHES
- URL: https://virusjour.crie.ru/jour/article/view/627
- DOI: https://doi.org/10.36233/0507-4088-135
- ID: 627
Cite item
Full Text
Abstract
Introduction. The variability of SARS-CoV-2 appeared to be higher than expected, the emergence of new variants raises concerns.
The aim of the work was to compare the pathogenicity of the Wuhan and BA.1.1/Omicron variants in BALB/c mice and Syrian hamsters.
Materials and methods. The study used strains of SARS-CoV-2: Dubrovka phylogenetically close to Wuhan-Hu-1, and LIA phylogenetically close to Omicron, BALB/c mice, transgenic mice B6.Cg-Tg(K18-ACE2)2Prlmn/HEMI Hemizygous for Tg(K18-ACE2)2Prlmn, Syrian golden hamsters. Animals were infected intranasally, pathogenicity was estimated by a complex of clinical, pathomorphological and virological methods.
Results. Comparative studies of SARS-CoV-2 Dubrovka and LIA strains on animal models demonstrated their heterogeneous pathogenicity. In parallel infection of BALB/c mice with Dubrovka and LIA variants, the infection proceeded without serious clinical signs and lung damage. Infection with the LIA strain resulted to a systemic disease with a high concentration of viral RNA in the lungs and brain tissues of animals. The presence of viral RNA in mice infected with the Dubrovka strain was transient and undetectable in the lungs by day 7 post-infection. Unlike the mouse model, in hamsters, the Dubrovka strain had a greater pathogenicity than the LIA strain. In hamsters infected with the Dubrovka strain lung lesions were more significant, and the virus spread through organs, in particular in brain tissue, was observed. In hamsters infected with the LIA strain virus was not detected in brain tissue.
Conclusion. The study of various variants of SARS-CoV-2 in species initially unsusceptible to SARS-CoV-2 infection is important for monitoring zoonotic reservoirs that increase the risk of spread of new variants in humans.
Full Text
Введение
SARS-CoV-2 – вирус зоонозного происхождения, вызвавший новую коронавирусную инфекцию в 2019 г. (COVID-19) в Ухане, Китайская Народная Республика [1, 2], откуда он быстро распространился по всему миру, и в марте 2020 г. Всемирная организация здравоохранения объявила пандемию. Изменчивость вируса оказалась выше ожидаемой, появление новых вариантов SARS-CoV-2 вызывало обеспокоенность тем, что потенциально они могут быть более заразными и (или) уклоняться от иммунных реакций, вызванных предыдущей инфекцией или вакцинацией [3, 4].
К настоящему времени наиболее широкое распространение [5–13] получил сильно мутировавший по сравнению с первоначальным вариантом Ухань вариант B.1.1.529 (омикрон), демонстрирующий беспрецедентное накопление мутаций в белке S, некоторые из которых связаны с повышенной трансмиссивностью и уклонением от антител [14–18]. Такие мутации могут изменить восприимчивость других видов-хозяев к вирусу, тем самым потенциально расширяя область его обитания в животных [19, 20], а также создать новые возможности для моделирования инфекции в них.
Модели лабораторных животных, которые воспроизводят клинические и патологические особенности COVID-19 у человека, являются инструментами для изучения патогенеза, механизмов и путей передачи возбудителя, Кроме того, моделированию новой коронавирусной инфекции и её последствий на животных, дальнейшему сопоставлению полученных в этой модели данных с клиническими наблюдениями принадлежит важнейшая роль в оценке эффективности противовирусных препаратов и вакцин.
Модель вирусной инфекции должна воспроизводить клинические признаки заболевания, его тяжесть и сопоставимый уровень вирусной репликации, а также у модельного животного должны быть клеточные рецепторы, аналогичные человеческим [21]. В качестве рецептора для взаимодействия с SARS-CoV-2 был идентифицирован человеческий ангиотензинпревращающий фермент 2 (angiotensin-converting enzyme 2 – ACE2) [20]. Ландшафт восприимчивых видов животных определяется мутациями S-белка, которые могут модулировать сродство с ACE2 [22]. Инбредные мыши (WT, BALB/c, C57BL6, 129S) поддерживают репликацию вируса штамма Ухань, но клинические признаки заболевания не выявляются. Была разработана специальная трансгенная модель мыши, имеющая рецептор ACE2, аналогичный человеческому [23], и в которой инфекция носит летальный характер. Однако экспрессируемый человеческий рецептор АСЕ2 в таких трансгенных мышах не является физиологическим, эти мыши труднодоступны и очень дороги. Появились сообщения о том, что новые варианты, такие как B.1.351 (бета) и B.1.1.529 (омикрон), могут заражать устойчивых к SARS-CoV-2 мышей дикого типа (WT) [24–27], однако полный анализ чувствительности in vivo этих вирусов к настоящему времени не проведён. В отличие от мышиной модели, у сирийских хомяков клиническая картина SARS-CoV-2, патология лёгких, включая пневмонию, наиболее близко воссоздаёт инфекцию у человека [28].
Изучение штаммов SARS-CoV-2 в этой модели выявило их гетерогенность и различную патогенность, при этом данные по варианту B.1.1.529 (омикрон) неоднозначны, отличаются в различных исследованиях и зависят от штамма [29–31]. Нами от пациентов с лабораторно-подтверждённой инфекцией COVID-19 были выделены и охарактеризованы штаммы Dubrovka, филогенетически близкий к штамму Ухань, и LIA, филогенетически близкий к штамму омикрон, однако их изучение в моделях лабораторных животных не проводилось и данные об их патогенности у животных отсутствуют.
Целью нашей работы являлось сравнение инфекционности штаммов Dubrovka (Ухань-подобного) и LIA (омикрон-подобного) SARS-CoV-2 в моделях мышей BALB/c и сирийских хомяков, характеристика патогенеза и прогрессирования инфекции в этих моделях.
Материалы и методы
Вирусы и клетки
В работе использовались лабораторные штаммы коронавируса SARS-CoV-2: Dubrovka (идент. № GenBank: MW514307.1, выделен от пациента 4 июня 2020 г., классификация по Pango B.1.1.317), филогенетически близкий к штамму Wuhan-Hu-1, идент. № GenBank: MN908947.3) [29] и LIA (идент. № GenBank: ON032858.1, выделен от пациента 27 января 2022 г., классификация по Pango BA.1.15), филогенетически близкий к штамму омикрон. Штаммы вирусов SARS-CoV-2 были выделены на культуре клеток Vero CCL81 из назофарингеальных мазков больных СOVID-19. Культивирование вирусов проводили на клетках эпителия почки африканской зелёной мартышки Vero CCL81 (ATСС) из коллекции Научно-исследовательского института вакцин и сывороток (НИИВС) имени И.И. Мечникова при 37 °C в питательной среде DMEM (Dulbecco’s modified Eagles medium) с L-глутамином (300 мкг/мл) и глюкозой 4,5 г/л, смесью антибиотиков (пенициллин 100 МЕ/мл и стрептомицин 100 мкг/мл) в атмосфере 5% СО2. Штамм Dubrovka прошёл 20 последовательных пассажей и вызывал выраженное цитопатогенное действие (ЦПД). Штамм LIA прошёл 5 последовательных пассажей и вызывал менее выраженное ЦПД с гибелью до 20% клеток через 96 ч после заражения. Образцы вирусного материала для проведения работы хранились при температуре –80 °C в виде аликвот. Для титрования вирусов для заражения животных, вирусного материала из лёгких животных и характеристики вирусов также использовали перевиваемую культуру клеток эпителия почки африканской зелёной мартышки Vero CCL81.
Животные и эксперименты с ними
В опытах использовали самок мышей линии BALB/c массой 12–14 г, полученных из питомника «Стезар» (Владимирская обл.), самок и самцов трансгенных мышей линии B6.Cg-Tg(K18-ACE2)2Prlmn/HEMI Hemizygous for Tg(K18-ACE2)2Prlmn (Jackson Immunoresearch, West Grove, PA, USA), а также самок сирийских золотистых хомяков массой 50–60 г, полученных из ФИБХ РАН «Питомник «Пущино» (р. п. Столбовая, Московская обл.). Содержание животных соответствовало правилам по устройству, оборудованию и содержанию экспериментально-биологических клиник. Кормили животных брикетированными кормами в соответствии с утверждёнными нормами. Все эксперименты были утверждены Этическим комитетом по работе с животными НИИВС имени И.И. Мечникова (протокол № 11 от 01.12.2021).
Мышей и хомяков заражали интраназально под лёгким эфирным наркозом в объёме 30 и 100 мкл соответственно на обе ноздри в указанных для каждого опыта дозах. За животными велось ежедневное наблюдение в течение последующих 4–7 дней, проводилось ежедневное взвешивание. Уменьшение или увеличение массы тела рассчитывалось отдельно для каждой мыши и выражалось в процентах. При этом за 100% принималась масса животного перед инфицированием. Для всех мышей одной группы определялось среднее значение процента потери или увеличения массы.
Получение лёгких и других органов животных
В указанные дни после инфицирования вирусом в каждой группе забивали по 3–4 мыши или хомяка и в стерильных условиях извлекали лёгкие, ткани головного мозга, другие органы. Органы трёхкратно промывали в растворе 0,01 М фосфатно-солевого буфера (ФСБ). Далее левые лёгкие, головной мозг и другие органы гомогенизировали и ресуспендировали в 1 мл холодного стерильного раствора 0,01М ФСБ. Суспензию осветляли от клеточного дебриса центрифугированием при 2000 g в течение 10 мин, супернатант использовали для определения инфекционного титра вируса в культуре клеток и проведения полимеразной цепной реакции (ПЦР). Хранение полученных образцов осуществлялось при –80 °C до постановки экспериментов. Правые лёгкие фиксировали в 10% растворе формалина для гистологических исследований.
Авторы подтверждают соблюдение институциональных и национальных стандартов по использованию лабораторных животных в соответствии с Consensus Author Guidelines for Animal Use (IAVES, 23 July, 2010). Протокол исследования одобрен Этическим комитетом организации (протокол № 11 от 01.12.2021).
Определение титра вируса в лёгких животных
Для определения инфекционного титра вируса из лёгких мышей или хомяков клетки Vero CCL81 рассаживали в 96-луночные планшеты фирмы Costar со средней плотностью 10 000 клеток на лунку и выращивали в среде DMEM в присутствии 5% фетальной сыворотки телят, 10 мМ глутамина и антибиотиков (пенициллин 100 МЕ/мл и стрептомицин 100 мкг/мл) до формирования полного монослоя (в течение 3 дней). Перед заражением вирусом культуру клеток 2 раза промывали средой DMEM без сыворотки. Готовили 10-кратные разведения каждой пробы вируса из лёгких с 10–1 до 10–7. Приготовленные разведения в объёме 200 мкл вносили в планшеты с культурой клеток и инкубировали в атмосфере 5% CO2 при 37 °C в течение 5 суток до появления ЦПД в клетках вирусного контроля. Расчёт титра вируса проводили с использованием формулы M.A. Ramakrishnan в программе Excel [30] и выражали в lg ТЦИД50 / 0,1 мл (тканевой цитопатической инфекционной дозы 50). Далее рассчитывали среднее значение титра для проб от мышей одной группы.
Количественное определение РНК коронавируса SARS-CoV-2 в органах животных методом ПЦР
Для выделения рибонуклеиновой кислоты (РНК) использовали осветлённые центрифугированием гомогенаты лёгких и других органов животных. Выделение вирусной РНК проводили коммерческим набором реагентов для экстракции ДНК/РНК из биологического материала «МагноПрайм ЮНИ» (ТУ 21.20.23-024-09286667-2018, ООО «НекстБио», Россия) в соответствии с инструкцией производителя.
Количественное определение РНК вируса SARS-CoV-2 проводили методом обратной транскрипции и ПЦР с детекцией в режиме реального времени (ОТ-ПЦР-РВ), как описано A.V. Gracheva и соавт. [31]. Для выявления вирусной РНК были использованы праймеры и зонды к гену N (нуклеокапсида) вируса COVID-19-N-F, COVID-19-N-R, COVID-19-N-P (таблица). Реакцию ОТ-ПЦР-РВ проводили с использованием реагентов «2,5х реакционная смесь для ПЦР-РВ с Tag-полимеразой» и «обратная транскриптаза MMLV» («Синтол», Россия). Реакционная смесь объёмом 25 мкл содержала по 10 пмоль каждого праймера и 5 пмоль зонда, 10 мкл 2,5х реакционной смеси с Taq-ДНК полимеразой, 0,6 мкл обратной транскриптазы. Температурно-временной режим: 45 °C – 10 мин (1 цикл); 95 °C – 5 мин (1 цикл); 95 °C – 5 сек, 55 °C – 45 сек (45 циклов). Учёт флуоресцентного сигнала проводили на канале FAM. Все олигонуклеотиды синтезированы в OOO «Синтол» (Россия) [31].
Таблица. Последовательности олигонуклеотидов, использованные в работе
Table. Oligonucleotide sequences used in the work
Название Name | Последовательность 5’–3’ Sequence 5’–3’ |
COVID-19-N-F | GCGTTCTTCGGAATGTCG |
COVID-19-N-R | TTGGATCTCTTTGTCATCCAATTTG |
COVID-19-N-P | FAM-AACGTGGTTGACCTACAGGT-BHQ1 |
COVN-PC | GCGTTCTTCGGAATGTCGCGCGCATTGGCATGGAAGTCACCTTCGGAACCTTCGGAACGGAACGTGTGTTGACACCTACAGGTGCCATCAAATTGGAATGACAAAGATCCAA |
Реакции ОТ и ПЦР-РВ проводили в амплификаторе «ДТпрайм-4» («ДНК-технология», Россия). Значение порогового цикла в ПЦР-РВ определялось автоматически с помощью программы RealTime_PCR v.7.7 («ДНК-Технология») на основе математического анализа формы кривой амплификации (метод геометрический, Cp). Для построения калибровочного графика использовали десятикратные разведения синтетического олигонуклеотида COVN-PC (таблица). Для расчёта концентрации вирусной РНК применяли тип анализа оптических данных «количественный со стандартами». Количество выражали в lg копий РНК в 1 мл гомогената соответствующего органа при изучении содержания вируса в крови животных в 1 мл сыворотки крови.
Гистологическое изучение лёгких животных
Для гистологического исследования правое лёгкое мышей фиксировали в 10% нейтральном забуференном формалине в течение 24 ч, обезвоживали и заливали в гистомикс. На этапе заливки материал ориентировали вдоль длинной оси. Cерийные срезы толщиной 3–5 мкм изготавливали на ротационном микротоме Leica RM 2125 RTS (Leica, Германия), затем окрашивали гематоксилином и эозином и заключали в канадский бальзам. Полученные гистологические препараты исследовали под световым микроскопом Olympus BX51 (Olympus, Япония) с системой фоторегистрации гистопрепаратов и обработки изображений.
Результаты
Сравнительное изучение патогенеза инфекции у мышей различных линий при заражении их вариантами SARS-CoV-2 Dubrovka (Ухань-подобным) и LIA (омикрон-подобным)
При изучении патогенеза инфекции при заражении штаммами Dubrovka (Ухань-подобным) и LIA (омикрон-подобным) были использованы мыши линии BALB/c. В качестве контрольных мышей при заражении штаммом Dubrovka (Ухань-подобным) использовали трансгенных мышей K18-hACE2, экспрессирующих человеческий ACE2-рецептор, используемый SARS-CoV-2 для проникновения в клетки. Состояние, смертность и массу животных контролировали ежедневно. При параллельном заражении мышей BALB/c штаммами Dubrovka и LIA в обоих случаях инфекция протекала без серьёзных клинических признаков болезни, смертности и практически без потери массы (рис. 1). Напротив, при заражении трансгенных мышей K18-hACE2 дозой 103,5 ТЦИД50 на 7-й день после инфицирования 3 из 7 животных погибли, а у оставшихся 4 фиксировалось тяжёлое состояние (низкая температура, невозможность принимать пищу и воду, потеря способности к движению) и потеря около 25% первоначальной массы. В связи с этим на основании Правил обращения с лабораторными животными они были гуманно умерщвлены и рассматривались как умершие в этот день. Таким образом, гибель всех животных в этой группе на 7-й день после заражения можно рассматривать как полную (100%,) потеря массы достигала максимума к этому дню, составляя примерно 25% (рис. 1).
Рис. 1. Показатели мышей линий BALB/c и K18-hACE2, заражённых штаммами Dubrovka и LIA: а – масса тела (линия показывает значение массы M ± SD); б – выживаемость; в – средние значения концентраций РНК SARS-CoV-2 в тканях различных органов мышей линии BALB/c, зараженных штаммами Dubrovka и LIA; г – инфекционный титр вируса (lg ТЦИД50/мл) и содержание вирусной РНК (lg копий РНК/мл) SARS-CoV-2 штамма Dubrovka в лёгких мышей K18-hACE2 на 4-й и 7-й день после инфицирования.
Изучение органов животных, взятых на 4-й день после инфицирования штаммом LIA (омикрон-подобным), выявило высокое содержание вирусной РНК в лёгких, тканях сердца, головного мозга и крови (на уровне 5,0–7,0 lg копий РНК/мл). При заражении штаммом Dubrovka (Ухань-подобным) вирусная РНК у мышей была преходящей: 2,1–2,5 lg копий РНК/мл Dubrovka против более 6 lg копий РНК/мл LIA на 4-й день после инфекции и не обнаруживалась в лёгких уже на 7-й день после заражения (рис. 1). Также не было выявлено вируса в тканях головного мозга и в крови. Напротив, при заражении этим же штаммом трансгенных мышей K18-hACE2, взятых в качестве контроля, титр вируса в лёгких был наибольшим на 4-й день после инфицирования (на 7-й день после инфекции титр был ниже, оставаясь относительно высоким – 6,9 ± 0,69 lg ТЦИД50 / 0,1 мл против 4,9 ± 0,57 lg ТЦИД50 / 0,1 мл). Высокие титры вируса в лёгких и других органах трансгенных мышей K18-hACE2 при заражении штаммом Dubrovka (Ухань-подобным) свидетельствуют об остром развитии системной инфекции, которая закончилась смертью животных.
Гистологическое исследование показало, что гистоструктура лёгких мышей BALB/c, инфицированных штаммом Dubrovka (Ухань-подобным), в целом соответствовала таковой у интактных мышей (рис. 2). Однако в лёгких мышей этой группы чаще, чем у незаражённых животных, встречались небольшие скопления лимфоцитов, располагавшиеся в стенке бронхов либо периваскулярно (рис. 2 в, г). Эти слабо выраженные воспалительные изменения, вероятно, являются иммунным ответом на антигенную стимуляцию и не оказывают значительного повреждающего действия. Несмотря на высокое содержание вируса в лёгких, при заражении мышей BALB/c вариантом LIA (омикрон-подобным) в различных дозах (от 103,5 до 104,5 lg ТЦИД50) признаки развития интерстициальной (вирусной) пневмонии, так же как и в случае заражения штаммом Dubrovka (Ухань-подобный), не обнаружены.
Рис. 2. Морфологическая характеристика лёгких интактных (а, б) и инфицированных штаммом Dubrovka (Ухань-подобным) (в, г) мышей линии BALB/c: а – просветы бронхов и бронхиол свободные, паренхима органа выглядит воздушной; б – просветы альвеол равномерно воздушные, межальвеолярные перегородки тонкие, сосуды и капилляры умеренно полнокровны; в – гистоструктура лёгкого соответствует варианту нормы; г – небольшое лимфоидное скопление (бронхо-ассоциированная лимфоидная ткань) в области контакта бронха и кровеносного сосуда. Увеличение: а, в – ×40; б – ×400; г – ×200; окрашивание: гематоксилин и эозин.
Сравнительное изучение патогенеза инфекции у золотистых сирийских хомяков при заражении их вариантами SARS-CoV-2 Dubrovka (Ухань-подобным) и LIA (омикрон-подобным)
Интраназальное заражение сирийских хомяков штаммом Dubrovka (Ухань-подобным) в дозе 104,5 ТЦИД50 вызывало снижение массы животных на 8–10% без проявления явных клинических признаков заболевания и смертности (рис. 3). Вирусологическое изучение органов хомяков , зараженных штаммом Dubrovka (Ухань-подобный), взятых на 4-й день после инфицирования, выявило высокую концентрацию РНК SARS-CoV-2 в лёгких (8,2 lg копий РНК/мл) и тканях головного мозга (7,7 lg копий РНК/мл). Кроме того, РНК надёжно определялась в тканях сердца и в крови (на уровне 6,5-6,7 lg копий РНК/мл) (рис. 3).
Заражение сирийских хомяков штаммом LIA (омикрон-подобным) в различных дозах (от 103,5 до 104,5 ТЦИД50) не вызывало видимых признаков заболевания и потери массы у животных (рис. 3). При вирусологическом изучении лёгких в них обнаружился одинаково высокий, не зависящий от дозы заражения уровень вирусной РНК (около 9 lg копий РНК/мл), однако вирус в тканях головного мозга и других органах практически определялся (рис. 3).
Рис. 3. Показатели золотистых сирийских хомяков, заражённых штаммами Dubrovka и LIA: a – масса тела (линия показывает значение массы M ± SD); б – средние значения концентраций РНК SARS-CoV-2 в тканях различных органов.
Макроскопическое сравнение лёгких сирийских хомяков выявило у инфицированных штаммом Dubrovka (Ухань-подобным) скопления и (или) кровоизлияния, которые отсутствовали у инфицированных LIA (омикрон-подобным). На микроскопическом уровне в гистологических препаратах лёгких у всех животных, инфицированных штаммом Dubrovka (Ухань-подобным), наблюдали выраженные воспалительные изменения, морфологическая картина которых соответствовала вирусной пневмонии. В некоторых долях лёгких площадь обширных сливных безвоздушных зон и прилегающих к ним участков со сниженной воздушностью, оценённая на качественном уровне, достигала 80% от площади доли (рис. 4 а, б). Воспалительные изменения в стенке бронхов и бронхиол, расположенных в очагах пневмонии, были незначительными. Лимфогистиоцитарный инфильтрат редко проникал глубже их адвентициальной оболочки. В их просвете содержались немногочисленные десквамированные эпителиоциты, единичные макрофаги и нейтрофилы. Сосуды в очагах пневмонии были полнокровны, окружены умеренно выраженным воспалительным инфильтратом из диффузно рассеянных лимфоцитов, гистиоцитов и небольшой примеси полиморфноядерных лейкоцитов. Наблюдали выраженный периваскулярный отёк.
Окружающая паренхима в лёгких животных, инфицированных штаммом Dubrovka (Ухань-подобным), представляла собой безвоздушные поля, в которых просвет альвеол не определялся, межальвеолярные перегородки были разрушены за счёт воспалительного инфильтрата, интерстициального отёка и гибели респираторного эпителия. Воспалительный инфильтрат состоял из гистиоцитов, лимфоцитов, единичных нейтрофилов, среди них были видны остатки ядер погибших клеток, островки пролиферирующего респираторного эпителия и фибробласты. Сосуды и капилляры были в состоянии резкого полнокровия. В прилегающих участках паренхимы со сниженной воздушностью отмечено утолщение межальвеолярных перегородок за счёт полнокровия микрососудов, интерстициального отёка и лимфогистиоцитарного инфильтрата. Просветы альвеол в этих участках содержали отёчную жидкость, эритроциты, единичные десквамированные альвеолоциты, макрофаги, лимфоциты, редко нити фибрина.
В лёгких всех хомяков, заражённых штаммом LIA (омикрон-подобным) в наиболее высокой из всех изученных доз (104,5 ТЦИД50), также развивались выраженные альтеративно-воспалительные изменения, соответствовавшие интерстициальной (вирусной) пневмонии, морфологическая картина которой была идентична таковой при заражении штаммом Dubrovka (Ухань-подобным). Однако в этом случае площадь крупных очагов пневмонии была значительно меньше, чем при заражении штаммом Dubrovka (Ухань-подобным) (не более 30–50% от площади гистологических срезов наиболее поражённых долей при заражении штаммом LIA (омикрон-подобным) против 80% при заражении штаммом Dubrovka (Ухань-подобным) (рис. 4). Несмотря на то что содержание вируса в лёгких хомяков, заражённых штаммом LIA (омикрон-подобным), при всех дозах заражения было примерно одинаковым, при гистологическом изучении было выявлено, что общая площадь очагов пневмонии, оценённая на качественном уровне, снижалась с уменьшением дозы заражения и составляла не более 15–20 и 5% от общей площади гистологического среза долей при заражении дозами 104 и 103,5 ТЦИД50 соответственно.
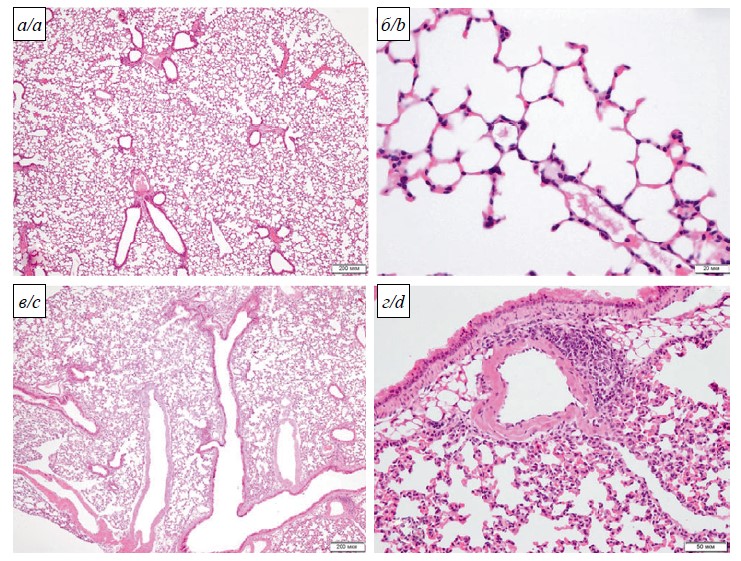
Рис. 4. Альтеративно-воспалительные изменения в лёгких сирийских хомяков на 4-е сутки после инфицирования SARS-CoV-2 штаммом Dubrovka (Ухань-подобным): а – сливные очаги вирусной пневмонии; б – перибронхиальный безвоздушный очаг пневмонии: просвет бронха свободный; эпителиальная выстилка сохранена, слабая воспалительная инфильтрация стенки бронха; в прилегающей паренхиме межальвеолярные перегородки разрушены за счёт воспалительного инфильтрата, отёка и гибели респираторного эпителия; в – участок паренхимы лёгкого со сниженной воздушностью: выраженный периваскулярный отёк, просветы альвеол щелевидные, в них отёчная жидкость, десквамированный эпителий, макрофаги, эритроциты, лимфоциты; г – участок паренхимы лёгкого со сниженной воздушностью: интраальвеолярный отёк, интраальвеолярные кровоизлияния, утолщённые за счёт лимфогистиоцитарного инфильтрата и интерстициального отёка, межальвеолярные перегородки, резкое полнокровие капилляров. Увеличение: а – ×40, в – ×200, б, г – ×400; окрашивание: гематоксилин и эозин.
Обсуждение
Ранее было показано, что различные линии инбредных мышей не восприимчивы к первоначальному штамму SARS-CoV-2, вызвавшему COVID-19. Ключевым рецептором при взаимодействии с SARS-CoV-2 у людей является ACE2, взаимодействие с которым происходит через рецептор-связывающий домен (RBD) S-белка вируса SARS-CoV-2. Мышиный ACE2 (mACE2) не допускает заражения SARS-CoV-2, что явилось основанием для использования специальной модельной трансгенной мыши K18-hACE2, экспрессирующей рецептор ACE2, аналогичный человеческому (hACE2) [23]. Полученные нами вирусологические и патологические характеристики показали, что штамм Dubrovka (Ухань-подобный) не вызывает продуктивной инфекции у мышей BALB/c, что совпадает с предыдущими исследованиями [24–27]. Напротив, при заражении штаммом LIA (омикрон-подобным) у мышей BALB/c наблюдалось размножение вируса в лёгких, тканях головного мозга, сердца, в крови. Важным аспектом этой инфекции являлось отсутствии смертности, явных клинических и неврологических проявлений и повреждения лёгких, выявляемых в гистологических исследованиях, в отличие от трансгенных мышей, экспрессирующих hACE2, у которых при заражении штаммом Dubrovka (Ухань-подобным) развилось тяжёлое клиническое течение, приводящее к смерти. Показано, что вариант омикрон также патогенен для трансгенных мышей K18-hACE2, однако потеря массы, смертность, воспалительные реакции выражены слабее, чем при инфицировании вариантом Ухань [29]. Наши результаты подтверждают данные об адаптации вируса к мышам, однако механизм этого процесса остаётся невыясненным. Молекулярные и генетические исследования показали, что наличие мутаций в S-гене у варианта BA.1 (омикрон) приводит к повышенному сродству только с рецептором mACE2, что даёт основание предполагать, что пониженная вирулентность этого штамма, вероятно, связана, помимо сродства RBD с ACE2, с другими факторами, в частности с более низкой фузогенностью [32, 33].
В наших экспериментах при параллельном моделировании инфекции обоими штаммами у сирийских хомяков мы не обнаружили значительных различий в концентрации вирусной РНК в лёгких на 4-й день после инфицирования. Однако у хомяков, инфицированных штаммом Dubrovka (Ухань-подобным), по данным гистологических исследований поражения лёгких были значительнее, наблюдались потеря массы и распространение вируса по органам. Наиболее значимым отличием между вариантами в модели сирийских хомяков было наличие инфекции в тканях головного мозга при заражении штаммом Dubrovka (Ухань-подобным), в то время как при заражении штаммом LIA (омикрон-подобным) вирус в тканях головного мозга не определялся. Таким образом, в отличие от мышиной модели, у сирийских хомяков штамм Dubrovka (Ухань-подобный) был более вирулентным, чем штамм LIA (омикрон-подобный), что сопоставимо с более лёгким течением болезни у людей, инфицированных коронавирусом BA.1 (омикрон).
Интересным фактом является то, что, несмотря на активное размножение вируса в лёгких сирийских хомяков при заражении обоими штаммами и мышей линии BALB/c при инфицировании штаммом LIA (омикрон-подобным), у заражённых животных не наблюдаются смертность и явные клинические и неврологические симптомы заболевания, что может быть обусловлено быстрым и эффективным иммунным ответом [34] или неспособностью вируса поддерживать множественные циклы репликации. Для лучшего понимания этого процесса необходимы дальнейшее изучение гуморального и клеточного иммунитета в этих моделях, корреляция их с вирусологическими, патоморфологическими, клиническими характеристиками и исследованиями у людей.
Заключение
Доброкачественное течение болезни, при которой, однако, фиксируется размножение вируса в лёгких, приводящее к развитию вирусной пневмонии, наблюдаемое нами на моделях сирийских хомяков и мышей линии BALB/c, сопоставимо с инфекцией, вызванной SARS-CoV-2 на других моделях животных, в частности у приматов и хорьков. Благоприятный исход заболевания как в этих моделях, так и у людей в конечном счёте устраняется действием иммунного ответа [34]. Наши данные об адаптации омикрон-подобного штамма SARS-CoV-2 к мышам в совокупности с этим обстоятельством вызывают опасения по поводу распространения тропизма новых вариантов к новым хозяевам, которые изначально были невосприимчивы к данной инфекции. Это создаёт потенциальный риск возникновения новых зоонозных резервуаров и распространения новых вариантов у людей, что диктует необходимость постоянного мониторинга возникающих вариантов SARS-CoV-2.
Участие авторов. Все авторы внесли существенный вклад в проведении экспериментов, поисково-аналитической работы и подготовку статьи, прочли и одобрили финальную версию до публикации.
Финансирование. Исследование выполнено за счет государственного бюджета.
Благодарность. Исследование выполнено с использованием оборудования Центра коллективного пользования ФГБНУ «Научно-исследовательский институт вакцин и сывороток имени И.И. Мечникова».
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Этическое утверждение. Авторы подтверждают соблюдение институциональных и национальных стандартов по использованию лабораторных животных в соответствии с Consensus Author Guidelines for Animal Use (IAVES, 23 July, 2010). Протокол исследования одобрен Этическим комитетом организации (протокол № 11 от 01.12.2021).
About the authors
Irina A. Leneva
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Author for correspondence.
Email: wnyfd385@yandex.ru
ORCID iD: 0000-0002-7755-2714
PhD (Bio.), head of Laboratory of Experimental Virology
Russian Federation, 105064, MoscowDaria I. Smirnova
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: daria.sm.1995@mail.ru
ORCID iD: 0000-0001-7325-0834
junior researcher, Laboratory of Molecular Virology
Russian Federation, 105064, MoscowNadezhda P. Kartashova
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: nadezdakartasova10571@gmail.com
ORCID iD: 0000-0003-2096-5080
researcher, Laboratory of Experimental Virology
Russian Federation, 105064, MoscowAnastasiia V. Gracheva
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: anastasiia.gracheva.95@mail.ru
ORCID iD: 0000-0001-8428-4482
junior researcher, Laboratory of Molecular Virology
Russian Federation, 105064, MoscowAnna V. Ivanina
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: ivanina.anna97@mail.ru
ORCID iD: 0000-0002-7289-693X
research laboratory assistant, Laboratory of Experimental Virology
Russian Federation, 105064, MoscowEkaterina A. Glubokova
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: eaglubokova@yandex.ru
ORCID iD: 0000-0002-5925-9733
junior researcher, Laboratory of Experimental Virology
Russian Federation, 105064, MoscowEkaterina R. Korchevaya
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: c.korchevaya@gmail.com
ORCID iD: 0000-0002-6417-3301
junior researcher, Laboratory of Molecular Virology
Russian Federation, 105064, MoscowAndrey A. Pancratov
Herzen Moscow Research Institute of Oncology of the Ministry of Health of Russia
Email: andreimnioi@yandex.ru
ORCID iD: 0000-0001-7291-9743
PhD, Head of the Department of Experimental Pharmacology and Toxicology
Russian Federation, 125284, MoscowGalina V. Trunova
Herzen Moscow Research Institute of Oncology of the Ministry of Health of Russia
Email: gtrunovamnioi@mail.ru
ORCID iD: 0000-0003-2917-4496
PhD, senior researcher of the Department of Experimental Pharmacology and Toxicology
Russian Federation, 125284, MoscowVarvara A. Khokhlova
Herzen Moscow Research Institute of Oncology of the Ministry of Health of Russia
Email: nostocus@yandex.ru
ORCID iD: 0000-0002-0339-2068
junior researcher of the Department of Experimental Pharmacology and Toxicology
Russian Federation, 125284, MoscowOksana A. Svitich
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: svitichoa@yandex.ru
ORCID iD: 0000-0003-1757-8389
D. Sci. (Med.), Prof., Corresponding Member of RAS, Head, Laboratory of molecular immunology, Director
Russian Federation, 105064, MoscowVitaly V. Zverev
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: vitalyzverev@outlook.com
ORCID iD: 0000-0001-5808-2246
D. Sci. (Biol.), Prof., Academician of RAS, Head, Laboratory of molecular biotechnology
Russian Federation, 105064, MoscowEvgeny B. Faizuloev
Mechnikov Research Institute of Vaccines and Sera, Department of Virology
Email: faizuloev@mail.ru
ORCID iD: 0000-0001-7385-5083
PhD (Biol.), Head of Molecular Virology Laboratory
Russian Federation, 105064, MoscowReferences
- Holmes E.C., Goldstein S.A., Rasmussen A.L., Robertson D.L., Crits-Christoph A., Wertheim J.O., et al. The origins of SARS-CoV-2: A critical review. Cell. 2021; 184(19): 4848–56. https://doi.org/10.1016/j.cell.2021.08.017
- Rasmussen A.L. On the origins of SARS-CoV-2. Nat. Med. 2021; 27(1): 9. https://doi.org/10.1038/s41591-020-01205-5
- Trinité B., Pradenas E., Marfil S., Rovirosa C., Urrea V., TarrésFreixas F., et al. Previous SARS-CoV-2 infection increases B.1.1.7 cross-neutralization by vaccinated individuals. Viruses. 2021; 13(6): 1135. https://doi.org/10.3390/v13061135
- Wang P., Nair M.S., Liu L., Iketani S., Luo Y., Guo Y., et al. Antibody resistance of SARS-CoV-2 variants B.1.351 and B.1.1.7. Nature. 2021; 593(7857): 130–5. https://doi.org/10.1038/s41586-021-03398-2
- Mullen J.L., Tsueng G., Latif A.A., Alkuzweny M., Cano M., Haag E., et al. Center for Viral Systems Biology. Outbreak.info. 2020. Available at: https://outbreak.info/
- Wang R., Chen J., Gao K., Hozumi Y., Yin C., Wei G.W. Analysis of SARS-CoV-2 mutations in the United States suggests presence of four substrains and novel variants. Commun. Biol. 2021; 4(1): 228. https://doi.org/10.1038/s42003-021-01754-6
- Dejnirattisai W., Zhou D., Supasa P., Liu C., Mentzer A.J., Ginn H.M., et al. Antibody evasion by the P.1 strain of SARS-CoV-2. Cell. 2021; 184(11): 2939–54.e9. https://doi.org/10.1016/j.cell.2021.03.055
- Planas D., Bruel T., Grzelak L., Guivel-Benhassine F., Staropoli I., Porrot F., et al. Sensitivity of infectious SARS-CoV-2 B.1.1.7 and B.1.351 variants to neutralizing antibodies. Nat. Med. 2021; 27(5): 917–24. https://doi.org/10.1038/s41591-021-01318-5
- Dhar M.S., Marwal R., Vs R., Ponnusamy K., Jolly B., Bhoyar R.C., et al. Genomic characterization and epidemiology of an emerging SARS-CoV-2 variant in Delhi, India. Science. 2021; 374(6570): 995–9. https://doi.org/10.1126/science.abj9932
- Parums D. Editorial: Revised World Health Organization (WHO) terminology for variants of concern and variants of interest of SARS-CoV-2. Med. Sci. Monit. 2021; 27: e933622. https://doi.org/10.12659/MSM.933622
- Karim S.S.A., Karim Q.A. Omicron SARS-CoV-2 variant: a new chapter in the COVID-19 pandemic. Lancet. 2021; 398(10317): 2126–8. https://doi.org/10.1016/S0140-6736(21)02758-6
- Allen H., Tessier E., Turner C., Anderson C., Blomquist P., Simons D., et al. Comparative transmission of SARS-CoV-2 Omicron (B.1.1.529) and Delta (B.1.617.2) variants and the impact of vaccination: national cohort study, England. medRxiv. 2022. Preprint. https://doi.org/10.1101/2022.02.15.22271001
- Lambrou A.S., Shirk P., Steele M.K., Paul P., Paden C.R., Cadwell B., et al. Genomic surveillance for SARS-CoV-2 variants: Predominance of the Delta (B.1.617.2) and omicron (B.1.1.529) variants – United States, June 2021 – January 2022. MMWR Morb. Mortal. Wkly Rep. 2022; 71(6): 206–11. https://doi.org/10.15585/mmwr.mm7106a4
- Petersen E., Ntoumi F., Hui D.S., Abubakar A., Kramer L.D., Obiero C., et al. Emergence of new SARS-CoV-2 Variant of Concern Omicron (B.1.1.529) – highlights Africa’s research capabilities, but exposes major knowledge gaps, inequities of vaccine distribution, inadequacies in global COVID-19 response and control efforts. Int. J. Infect. Dis. 2022; 114: 268–72. https://doi.org/10.1016/j.ijid.2021.11.040
- Andrews N., Stowe J., Kirsebom F., Toffa S., Rickeard T., Gallagher E., et al. Covid-19 vaccine effectiveness against the omicron (B.1.1.529) variant. N. Engl. J. Med. 2022; 386(16): 1532–46. https://doi.org/10.1056/NEJMoa2119451
- Grabowski F., Kochańczyk M., Lipniacki T. The spread of SARS-CoV-2 variant omicron with a doubling time of 2.0-3.3 days can be explained by immune evasion. Viruses. 2022; 14(2): 294. https://doi.org/10.3390/v14020294
- Liu L., Iketani S., Guo Y., Chan J.F.W., Wang M., Liu L., et al. Striking antibody evasion manifested by the Omicron variant of SARS-CoV-2. Nature. 2022; 602(7898): 676–81. https://doi.org/10.1038/s41586-021-04388-0
- Planas D., Saunders N., Maes P., Guivel-Benhassine F., Planchais C., Buchrieser J., et al. Considerable escape of SARS-CoV-2 Omicron to antibody neutralization. Nature. 2022; 602(7898): 671–5. https://doi.org/10.1038/s41586-021-04389-z
- Conceicao C., Thakur N., Human S., Kelly J.T., Logan L., Bialy D., et al. The SARS-CoV-2 Spike protein has a broad tropism for mammalian ACE2 proteins. PLoS Biol. 2020; 18(12): e3001016. https://doi.org/10.1371/journal.pbio.3001016
- Liu Y., Hu G., Wang Y., Ren W., Zhao X., Ji F., et al. Functional and genetic analysis of viral receptor ACE2 orthologs reveals a broad potential host range of SARS-CoV-2. Proc. Natl Acad. Sci. USA. 2021; 118(12): e2025373118. https://doi.org/10.1073/pnas.2025373118
- Gretebeck L.M., Subbarao K. Animal models for SARS and MERS coronaviruses. Curr. Opin. Virol. 2015; 13: 123–9. https://doi.org/10.1016/j.coviro.2015.06.009
- Garry R.F. Mutations arising in SARS-CoV-2 spike on sustained human-to-human transmission and human-to-animal passage. Virological. 2021. Available at: https://virological.org/t/mutations-arising-in-sars-cov-2-spike-on-sustained-human-to-human-transmission-and-human-to-animal-passage/578/14
- Bao L., Deng W., Huang B., Gao H., Liu J., Ren L., et al. The pathogenicity of SARS-CoV-2 in hACE2 transgenic mice. Nature. 2020; 583(7818): 830–3. https://doi.org/10.1038/s41586-020-2312-y
- Kant R., Kareinen L., Smura T., Freitag T.L., Jha S.K., Alitalo K., et al. Common laboratory mice are susceptible to infection with the SARS-CoV-2 beta variant. Viruses. 2021; 13(11): 2263. https://doi.org/10.3390/v13112263
- Montagutelli X., Prot M., Levillayer L., Salazar E.B., Jouvion G., Conquet L., et al. bioRxiv. 2021. Preprint. https://doi.org/10.1101/2021.03.18.436013
- Shuai H., Chan J.F.W., Yuen T.T.T., Yoon C., Hu J.C., Wen L., et al. Emerging SARS-CoV-2 variants expand species tropism to murines. EBioMedicine. 2021; 73: 103643. https://doi.org/10.1016/j.ebiom.2021.103643
- Zhang Y.N., Zhang Z.R., Zhang H.Q., Li N., Zhang Q.Y., Li X.D., et al. Different pathogenesis of SARS-CoV-2 Omicron variant in wild-type laboratory mice and hamsters. Signal Transduct. Target. Ther. 2022 Feb 25; 7(1): 62. https://doi.org/10.1038/s41392-022-00930-2
- Imai M., Iwatsuki-Horimoto K., Hatta M., Loeber S., Halfmann PJ., Nakajima N., et al. Syrian hamsters as a small animal model for SARS-CoV-2 infection and countermeasure development. Proc. Natl Acad. Sci USA. 2020; 117(28): 16587–95. https://doi.org/10.1073/pnas.2009799117
- Gracheva A.V., Korchevaya E.R., Kudryashova A.M., Borisova O.V., Petrusha O.A., Smirnova D.I., et al. Adaptation of the MTT assay for detection of neutralizing antibodies against the SARS-CoV-2 virus. Zhurnal mikrobiologii, epidemiologii i immunobiologii. 2021; 98(3): 253–65. https://doi.org/10.36233/0372-9311-136 (in Russian)
- Ramakrishnan M.A. Determination of 50% endpoint titer using a simple formula. World J. Virol. 2016; 5(2): 85–6. https://doi.org/10.5501/wjv.v5.i2.85
- Gracheva A.V., Korchevaya E.R., Ammour Y.I., Smirnova D.I., Sokolova O.S., Glukhov G.S., et al. Immunogenic properties of SARS-CoV-2 inactivated by ultraviolet light. Arch. Virol. 2022; 167(11): 2181–91. https://doi.org/10.1007/s00705-022-05530-7
- Meng B., Abdullahi A., Ferreira I.A.T.M., Goonawardane N., Saito A., Kimura I., et al. Altered TMPRSS2 usage by SARS-CoV-2 Omicron impacts infectivity and fusogenicity. Nature. 2022; 603(7902): 706–14. https://doi.org/10.1038/s41586-022-04474-x
- Suzuki R., Yamasoba D., Kimura I., Wang L., Kishimoto M., Ito J., et al. Attenuated fusogenicity and pathogenicity of SARS-CoV-2 Omicron variant. Nature. 2022; 603(7902): 700–5. https://doi.org/10.1038/s41586-022-04462-1
- Kim Y.I., Kim S.G., Kim S.M., Kim E.H., Park S.J., Yu K.M., et al. Infection and rapid transmission of SARS-CoV-2 in ferrets. Cell Host Microbe. 2020; 27(5): 704–9.e2. https://doi.org/10.1016/j.chom.2020.03.023
Supplementary files