Том 66, № 5 (2021)
- Год: 2021
- Выпуск опубликован: 04.11.2021
- Статей: 7
- URL: https://virusjour.crie.ru/jour/issue/view/52
Весь выпуск
ОБЗОРЫ
Роль противовирусной терапии в лечении больных циррозом печени, ассоциированным с хронической HBV- и HCV-инфекцией
Аннотация
Формирование цирроза печени (ЦП) служит неблагоприятным событием естественного течения её хронических заболеваний и может сопровождаться осложнениями, которые нередко становятся причиной фатального исхода. Изучение эффективности лекарственных средств (ЛС), влияющих на различные этиопатогенетические механизмы этого состояния, представляет собой одну из актуальных проблем современной гепатологии. Цель обзора – показать роль противовирусной терапии (ПВТ) в лечении ЦП, ассоциированного с хронической инфекцией, вызываемой вирусами гепатитов В (hepatitis B virus, HBV) и С (hepatitis C virus, HCV).
Для поиска научных статей использовались база данных PubMed, поисковая система Google Scholar, Кокрейновские систематические обзоры, электронная научная библиотека eLIBRARY.RU, а также пристатейные списки литературы. В соответствии с задачами работы отбирались публикации за период 2000–2021 гг. по поисковым запросам: «цирроз печени»; «фиброз печени»; «хроническая HBV-инфекция»; «хроническая HCV-инфекция»; «портальная гипертензия»; «лечение». Критерии включения ограничивались проблемой терапии ЦП, ассоциированного с хронической HBV- и HCV-инфекцией.
Текущие гайдлайны рекомендуют бессрочное лечение пациентов с HBV-ассоциированным ЦП аналогами нуклеозидов/нуклеотидов (АН/Н) независимо от сывороточных уровней ДНК HBV; стандартом же терапии HСV-ассоциированного ЦП стала современная концепция использования комбинаций противовирусных препаратов прямого действия. Исследования показали способность ПВТ ингибировать и реверсировать фибротические процессы, что, в свою очередь, может уменьшить выраженность портальной гипертензии (ПГ) и снизить риск связанных с ней осложнений, а также нормализовать печёночную функцию. Кроме того, отмечается, что осуществление перед ортотопической трансплантацией печени (ОТП) эрадикации HBV/ HCV повышает общую выживаемость в долгосрочной перспективе. Таким образом, обеспечение доступности препаратов для нуждающихся в данных лечебных мероприятиях будет способствовать не только профилактике ЦП, но также позволит улучшить качество и увеличить продолжительность жизни страдающих им пациентов.
 331-339
331-339


Дельта-подобные вирусы (Kolmioviridae: Deltavirus) животных и происхождение вируса гепатита D (hepatitis D virus) человека
Аннотация
Вирус гепатита D (дельта, δ) (hepatitis D virus, HDV) открыт более 40 лет назад, однако представления о его происхождении и эволюции крайне ограничены. Причиной этому служило отсутствие до недавнего времени данных о существовании каких-либо вирусов, подобных HDV. Обнаружение в последние годы последовательностей новых дельта-подобных вирусов у широкого спектра представителей позвоночных (Vertebrata) и беспозвоночных (Invertebrata) позволило пересмотреть взгляды на возникновение HDV и способствовало пониманию места этого уникального вируса среди зоонозных инфекционных агентов вирусной природы. Целью данного обзора является анализ недавно опубликованных исследований, посвящённых новым дельта-подобным вирусам и их биологической характеристике.
 340-345
340-345


ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Определение уровня иммунной прослойки населения Гвинейской Республики к некоторым арбовирусам
Аннотация
Введение. Ежегодно в странах Западной Африки от острых лихорадочных заболеваний погибают свыше 250 тыс. человек. Бо́льшую часть в общей структуре регистрируемых лихорадок традиционно занимают малярия и брюшной тиф. Однако эти сведения не в полной мере отражают реальные данные обо всей конъюнктуре заболеваемости в западноафриканском регионе. Это связано с тем, что в качестве критериев постановки диагноза используются только клинические признаки инфекционного процесса, и не исключена вероятность того, что некоторое количество заболеваний может быть вызвано арбовирусами. Выявление специфических антител (АТ) к возбудителям инфекционных болезней в сыворотках крови жителей той или иной местности является достоверным показателем циркуляции этих патогенов на определённой территории.
Цель работы – определение уровня иммунной прослойки населения Гвинейской Республики (Гвинеи) к ряду арбовирусов: денге (DENV), Западного Нила (WNV, ВЗН) (семейство Flaviviridae); Крымской-Конго геморрагической лихорадки (CCHFV, ККГЛ), Батаи (Batai virus), Бханджа (BHAV) (порядок Bunyavirales); чикунгунья (CHIKV) и Синдбис (SINV) (семейство Togaviridae).
Материал и методы. Для работы собрана панель из 2620 образцов сывороток крови людей, проживающих во всех ландшафтно-географических зонах Гвинеи. Выявление АТ класса IgG проводилось с помощью иммуноферментного анализа (ИФА).
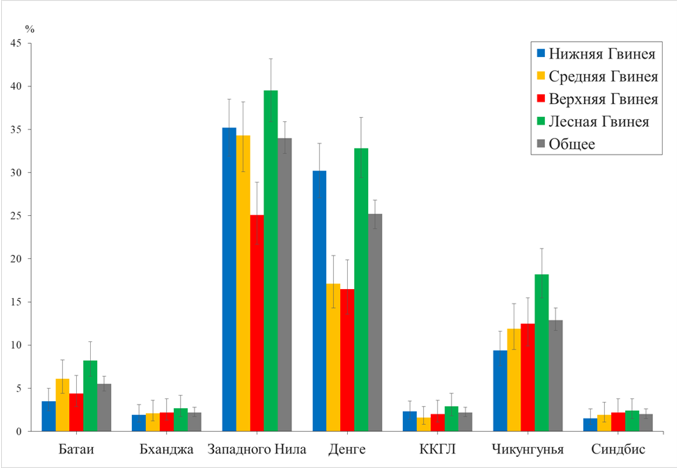
Результаты. Всего за период исследования АТ к вирусу Батаи выявлены в 144 (5,5%) образцах; Бханджа – в 58 (2,2%); ВЗН – в 892 (34,0%); денге – в 659 (25,2%); ККГЛ – в 58 (2,2%); чикунгунья – в 339 (12,9%) и Синдбис – в 52 образцах (2,0%).
Обсуждение. Полученные результаты указывают на наличие иммунной прослойки населения всех ландшафтно-географических зон Гвинейской Республики к данному спектру арбовирусов, что является подтверждением их активной циркуляции на этой территории.
Заключение. С учётом эпидемиологической значимости арбовирусных инфекций сохраняется актуальность дальнейшего изучения вопроса о доле инфекционных агентов этой экологической группы в общей структуре лихорадочных заболеваний, зарегистрированных на территории Гвинеи.
 346-353
346-353


Оптимизация схемы вакцинации собак против бешенства (Rhabdoviridae: Lyssavirus) при помощи математической модели
Аннотация
Введение. Большинство случаев бешенства (Rhabdoviridae: Lyssavirus) у людей вызвано укусами домашних и диких собак (Canis lupus familiaris). В этой связи одной из актуальных задач является организация программ массовой вакцинации этих животных.
Цель работы – выявить факторы, влияющие на синтез вируснейтрализующих антител (ВНА) к вирусу бешенства у вакцинированных собак, сформировать рекомендации по корректировке схемы вакцинации с использованием методов математического моделирования (ММ).
Материал и методы. Разработана двухкомпартментная математическая модель, параметры которой откалиброваны на лог-трансформированных данных о содержании ВНА в сыворотке крови вакцинированных собак с использованием нелинейного моделирования с фиксированными эффектами. Результаты получены методами RFFIT (rapid fluorescent focus inhibition test, анализ быстрого ингибирования фокусов флюоресценции) и FAVN (fluorescent antibody virus-neutralization test, тест нейтрализации вируса флюоресцентными антителами).
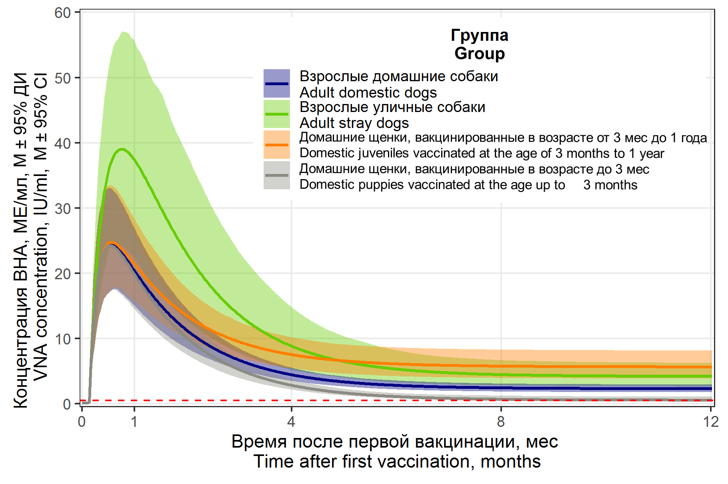
Результаты. Установлено, что при двукратной первичной вакцинации у щенков в возрасте от 3 мес до 1 года формируется более напряжённый иммунный ответ по сравнению с таковым у взрослых особей. При первичной вакцинации и ревакцинации спустя 1 год и более ВНА у взрослых уличных собак синтезируются более интенсивно, чем у домашних.
Обсуждение. Менее длительный иммунный ответ у животных, вакцинированных в возрасте до 3 мес, объясняется как наличием колостральных антител, так и активным развитием организма в этот период. Результаты наших исследований и данные работ других авторов подтверждают наличие у большинства собак протективного уровня ВНА к вирусу бешенства ≥0,5 МЕ/мл на протяжении 2 и более лет после вакцинации. Однако лишь регулярная ежегодная ревакцинация способствует достижению и поддержанию этого показателя у особей, плохо отвечающих на вакцинацию в силу различных факторов.
Заключение. Рекомендована следующая схема вакцинации собак против бешенства: первичное введение вакцинного препарата в возрасте от 3 мес до 1 года с 1–2-месячным интервалом, в дальнейшем ежегодная ревакцинация. Настоящая работа демонстрирует возможность более широкого применения методов ММ для решения задач вакцинопрофилактики.
 354-367
354-367


Противовирусная активность комплексного германийорганического соединения ацикловира в системах in vitro и in vivo в отношении вируса простого герпеса (Herpesviridae: Alphaherpesvirinae: Simplexvirus: Human alphaherpesvirus 1/2)
Аннотация
Введение. Значительный рост заболеваемости различными формами герпесвирусной инфекции (ГВИ) диктует необходимость поиска новых подходов к модификации одного из базовых противовирусных препаратов ацикловира (АЦВ) (Aciclovir; ACV) и его лекарственных форм с целью улучшения их биофармацевтических характеристик и повышения эффективности терапии. Одним из перспективных в данном аспекте является комплексное германийорганическое соединение ацикловира (КГОСА).
Цель исследования – изучение противовирусной активности КГОСА в отношении вируса простого герпеса (ВПГ) (герпесвируса человека, ГВЧ) (Herpesviridae: Alphaherpesvirinae: Simplexvirus: Human alphaherpesvirus 1/2) на моделях ГВИ in vitro и in vivo.
Материал и методы. С использованием вирусологического и статистического методов изучена активность КГОСА в лечебной схеме в отношении ВПГ 1 типа (ВПГ-1) (ГВЧ-1) (штамм «Кл»), ВПГ-2 (ГВЧ-2) (штамм «ВН») на моделях ГВИ in vitro на культуре клеток Vero и генитального герпеса (ГГ), вызванного ВПГ-2 (штамм «ВН»), у самцов морских свинок (Canis porcellus).
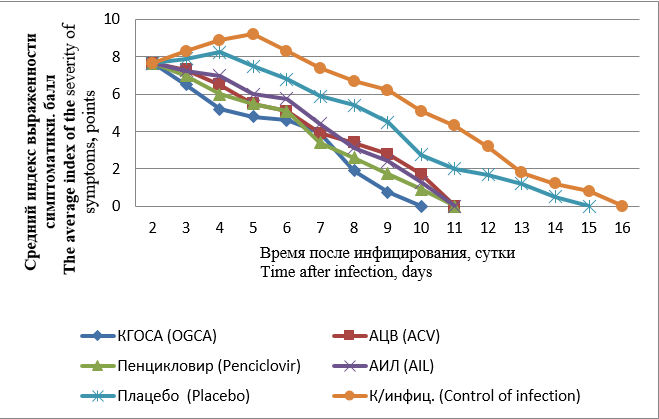
Результаты и обсуждение. Установлено, что КГОСА ингибирует репликацию ВПГ-1 и ВПГ-2 в клетках Vero. На модели ГГ у инфицированных животных препарат также обладает анти-ВПГ-активностью, приводящей к уменьшению выраженности симптоматики, тяжести и продолжительности заболевания, интенсивности и длительности выделения вируса. Наиболее выраженная активность соединения выявлена при применении в виде геля 3% местно 5 раз в день в течение 5 сут на ранних сроках после заражения. Отсроченное использование КГОСА (через 48 ч после инфицирования) также демонстрировало статистически значимую эффективность, сравнимую с таковой коммерческих референс-препаратов, в т.ч. содержащих АЦВ или его пролекарства: ацикловир (крем 5%), АИЛ (ацикловир+интерферон альфа-2b+лидокаин, мазь 3%), пенцикловир (крем 1%). КГОСА значимо снижал выраженность симптомов ГГ, уменьшал период вирусовыделения, а также инфекционную активность возбудителя по сравнению с этими параметрами у животных группы контроля и особей, получавших плацебо. Активность препарата, по-видимому, обусловлена его улучшенными биофармацевтическими характеристиками относительно АЦВ, а также наличием ряда биологических активностей у входящих в его состав компонентов.
Заключение. Результаты исследования позволяют рассматривать КГОСА как основу для разработки терапевтических средств для ГВИ, обладающих противовирусной активностью.
 368-382
368-382


Получение вирусоподобных частиц норовируса (Caliciviridae: Norovirus), содержащих белок VP1 энтеровируса Echovirus 30 (Picornaviridae: Enterovirus: Enterovirus B)
Аннотация
Введение. Энтеровирусная (неполио) инфекция имеет широкое распространение во всём мире, регистрируется в форме спорадической заболеваемости и масштабных вспышек и может быть причиной такого тяжёлого поражения, как серозный менингит. Эпидемиологические исследования показали, что на территории Российской Федерации у больных энтеровирусным менингитом наиболее часто выявляется вариант энтеровируса (ЭВ) (Picornaviridae; Enterovirus) Echovirus 30 (Е30). Однако вакцины для профилактики заболевания, вызванного этим возбудителем, до настоящего времени не разработаны. Одним из перспективных современных направлений в плане создания вакцинных препаратов является использование вирусоподобных частиц (ВпЧ), в т.ч. химерных – содержащих биологические структуры вирусов, принадлежащих к различным видам.
Цель настоящей работы – получение ВпЧ норовируса (Caliciviridae; Norovirus), содержащих на своей поверхности белок VP1 Е30.
Материал и методы. В работе использовали нуклеотидные последовательности генов белков VP1 норовируса генотипа GII.4 и VP1 вируса E30 генотипа h, циркулирующих на территории России. На их основе сконструирован белок SN-VP1E30, в котором оболочечный (S) и шарнирный (hinge) регионы VP1 норовируса слиты в одну молекулу с полноразмерным VP1 E30. Данный белок экспрессировали в E. coli, очищали методом аффинной хроматографии, после чего характеризовали с использованием электрофореза в полиакриламидном геле (ПААГ) и иммуноблоттинга. ВпЧ визуализировали методом электронной микроскопии.
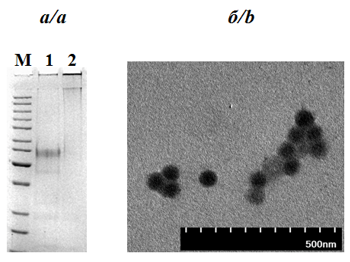
Результаты. Белок SN-VP1E30 экспрессировался в E. coli в нерастворимой форме. Подбор условий для получения его растворимой формы показал, что использование высоких концентраций сахарозы существенно повышает эффективность ренатурации. При сравнении электрофоретической подвижности денатурированного и неденатурированного препаратов SN-VP1E30 установлено, что большинство мономеров образуют соединения со значительной молекулярной массой. С помощью электронной микроскопии показано, что ренатурированный белок SN-VP1E30 самопроизвольно формирует in vitro полые ВпЧ диаметром ~50 нм.
Заключение. Показана возможность получения in vitro химерных ВпЧ норовируса, содержащих на своей поверхности белок VP1 циркулирующего на территории РФ варианта E30. Полученные частицы в дальнейшем могут быть использованы в разработке вакцинных препаратов для профилактики серозного менингита и других заболеваний, вызванных данным ЭВ.
 383-389
383-389


ЮБИЛЕЙНЫЕ ДАТЫ
 390-392
390-392