Том 66, № 1 (2021)
- Год: 2021
- Дата публикации: 07.03.2021
- Статей: 9
- URL: https://virusjour.crie.ru/jour/issue/view/48
Весь выпуск
ОБЗОРЫ
Вирус Эбола (Filoviridae: Ebolavirus: Zaire ebolavirus): фатальные адаптационные мутации
Аннотация
Болезнь, вызванная вирусом Эбола (БВВЭ) (прежнее название - геморрагическая лихорадка Эбола), - одно из самых опасных инфекционных заболеваний, поражающих человека и приматов. С момента идентификации первой вспышки в 1976 г. в мире зарегистрировано более 25 аналогичных эпизодов, самый крупный из которых в 2014-2016 гг. перерос в эпидемию и унёс жизни свыше 11 тыс. человек. В настоящее время одновременно в восточной и западной частях Демократической Республики Конго (ДРК) протекают 2 независимые вспышки БВВЭ. Считается, что естественным резервуаром её возбудителей являются летучие мыши (Microchiroptera), однако инфекционный агент из них до сих пор не выделен. Известно, что большинство вирусов животных не способно реплицироваться в человеческом организме. Для того чтобы произошло заражение человека, необходимо наличие адаптационных мутаций (АМ). В данном обзоре на основании результатов ряда исследований сформулирована гипотеза о том, что формирование мутационных изменений подобного рода происходит непосредственно в популяциях людей и приматов, приводя в дальнейшем к развитию вспышек БВВЭ.
 7-16
7-16


Экспресс-диагностика новой коронавирусной инфекции с помощью реакции петлевой изотермической амплификации
Аннотация
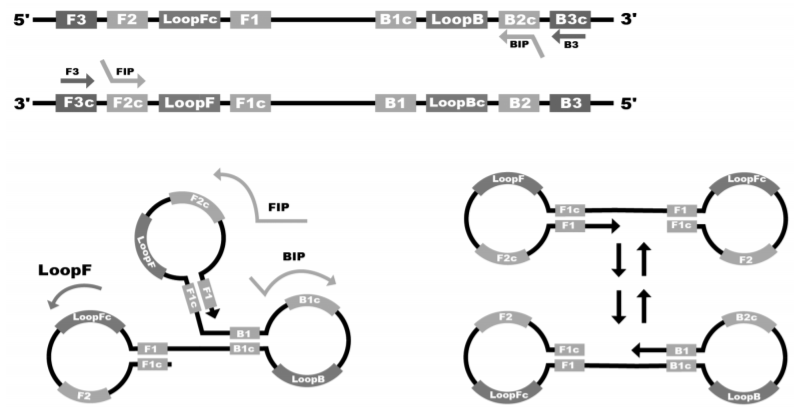
В настоящем обзоре представлены основные принципы применения реакции петлевой изотермической амплификации (loop-mediated isothermal amplification, LAMP) для экспресс-диагностики коронавирусной инфекции, вызванной SARS-CoV-2. Кратко описаны базовые технические детали метода, наиболее популярные способы специфической и неспецифической детекции продуктов амплификации, обсуждены первые опубликованные работы по использованию рассматриваемой технологии для выявления фрагментов молекулы нуклеиновой кислоты вируса SARS-CoV-2, в том числе разрабатываемые в Российской Федерации. Для доступных тестов на базе LAMP перечислены основные аналитические характеристики наборов, которые нередко сравнимы с параметрами тест-систем на основе метода полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР), а в ряде случаев превосходят их. Обсуждены преимущества и ограничения этого подхода в сравнении с другими способами молекулярной диагностики (в первую очередь ОТ-ПЦР), а также перспективы развития технологии для выявления возбудителей других инфекций.
 17-28
17-28


ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Биологическая характеристика и пермиссивность к вирусам штамма диплоидных клеток почки летучей мыши нетопыря Натузиуса (Pipistrellus nathusii Keyserling & Blasius, 1839; (Chiroptera: Microchiroptera: Vespertilionidae)
Аннотация
Введение. Летучие мыши (Microchiroptera) являются эпидемиологически важным естественным резервуаром вирусов различных таксономических групп, включая возбудителей особо опасных болезней человека и животных. Учитывая актуальность арбовирусных инфекций, представляется целесообразным проведение исследований по изучению спектра чувствительности клеток из тканей летучих мышей, обитающих и мигрирующих на территории Российской Федерации, к вирусам векторных инфекций сельскохозяйственных животных.
Цель исследования - получение диплоидного штамма клеток почечной ткани летучей мыши (ПЛМ) вида нетопырь лесной, или нетопырь Натузиуса (Pipistrellus nathusii), изучение его биологических характеристик, а также оценка пермиссивности полученной клеточной культуры к вирусам блютанга, лихорадки долины Рифт (ЛДР), заразного узелкового дерматита (ЗУД) крупного рогатого скота (КРС), миксомы кроликов (Myxomatosis cuniculi), фибромы Шоупа, африканской чумы лошадей (АЧЛ) и африканской чумы свиней (АЧС).
Материал и методы. Донорами органов служили 2 особи клинически здоровых самцов летучей мыши Р. nathusii. Для получения диплоидного штамма культуры клеток почки этого вида и изучения свойств полученной клеточной культуры градации от 6-го и выше пассажных уровней использовали традиционные цитологические, вирусологические и молекулярные методы. Определяли пермиссивность данного штамма к вирусам блютанга, ЛДР, ЗУД, миксомы кроликов, фибромы Шоупа, АЧЛ и АЧС.
Результаты. Формирование конфлюэнтного монослоя наблюдали через 72 ч, при этом индекс пролиферации (ИП) был равен 2,7-3,3. Клеточный монослой сохранялся без смены среды в течение 45 сут (срок наблюдения). Показана стабильность кариотипа в условиях непрерывного субкультивирования на уровне 36-го пассажа. Культура клеток получила наименование «Штамм диплоидных клеток почки летучей мыши Pipistrellus nathusii (Diploid cell line Pipistrellus nathusii kidney)»; установлена её пермиссивность к вирусам блютанга, ЛДР, ЗУД и миксомы кроликов.
Обсуждение. Чувствительность полученного клеточного материала к вирусам блютанга и ЛДР согласуется с данными об идентификации реовируса и возбудителя ЛДР у египетских фруктовых летучих мышей (Rousettus aegyptiacus), а пермиссивность данного штамма к возбудителям ЗУД и миксомы кроликов - с результатами обнаружения поксвирусов у вида поздний кожан (Eptesicus fuscus).
Выводы. Получен и паспортизирован штамм диплоидных клеток ПЛМ P nathusii. Установленная пермиссивность к вирусам блютанга, ЛДР, ЗУД и миксомы кроликов позволяет использовать его для выделения и изучения этих патологических агентов. Репродукция возбудителей в клетках данного штамма из тканей ПЛМ вида P nathusii, обитающего и мигрирующего на территории европейской части Российской Федерации, указывает на его потенциальную роль в эпидемиологии значимых инфекций, особенно трансмиссивных.
 29-39
29-39


Влияние антикоагулянтной терапии на течение COVID-19 у коморбидных пациентов
Аннотация
Введение. Анализ патогенеза новой коронавирусной инфекции свидетельствует о значительном влиянии нарушений гемореологии на её течение и исходы. Известно, что хронические заболевания сердечно-сосудистой системы ассоциируются с риском тяжёлого течения и летальных исходов как при COVID-19, так и при других инфекционных болезнях. В связи с этим в каждом случае необходимо изучение взаимодействия и взаимовлияния различных составляющих лечебной программы, назначаемой таким пациентам.
Цель работы - оценить влияние активности системы гемокоагуляции на течение новой коронавирусной инфекции (COVID-19) и обосновать тактику ведения коморбидных пациентов, получающих новые пероральные антикоагулянты (ПОАК) в подобранных ранее дозах по имеющимся показаниям в связи с наличием тех или иных соматических заболеваний.
Материал и методы. Проанализировано 76 случаев подтверждённой коронавирусной инфекции у пациентов, получавших стартовую терапию ПОАК (ривароксабан, апиксабан, дабигатран) амбулаторно. Из этого количества 26 участников, принимавших данные препараты, составили основную группу, и 50 - группу сравнения (контрольную), в которой до эпизода COVID-19 не назначались лекарственные средства, влияющие на свёртываемость крови. Всем пациентам было проведено лечение в соответствии с актуальной на момент начала исследования версией Временных методических рекомендаций «Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19)» (https://static-0.minzdrav.gov.ru/system/attachments/attaches/).
Результаты и обсуждение. В группе пациентов, которым назначались ПОАК, отмечено достоверно меньшее число случаев госпитализаций (19 против 66% в контрольной группе), отсутствие летальных исходов и эпизодов развития тяжёлой дыхательной и/или почечной недостаточности, тогда как среди не получавших антикоагулянты неблагоприятные исходы зарегистрированы в 14%.
Заключение. Приём ПОАК в соответствии с имеющейся сопутствующей патологией соматического характера снижает вероятность тяжёлого течения и неблагоприятных исходов при развитии инфекции, вызванной SARS-CoV-2, что указывает на существенный вклад поражения различных звеньев свёртывающей системы крови в патогенез COVID-19. У пациентов, получающих адекватную терапию указанными препаратами, при лечении в амбулаторных условиях лёгкой и среднетяжёлой форм коронавирусной инфекции не выявлено показаний для замены лекарственных средств этой фармакологической группы и коррекции схем антикоагулянтной терапии.
 40-46
40-46


Интерферон гамма в терапии пациентов с COVID-19 среднетяжёлого течения
Аннотация
Введение. Интерфероны вырабатываются в ответ на внедрение патогена в клетку и отвечают за правильное формирование иммунного ответа. Предварительные исследования с участием пациентов с внебольничной пневмонией (в т.ч. бактериального генеза), острой респираторной вирусной инфекцией (ОРВИ), гриппом и новой коронавирусной инфекцией COVID-19 по изучению свойств рекомбинантного интерферона гамма (ИФН-γ) показали обнадёживающие результаты.
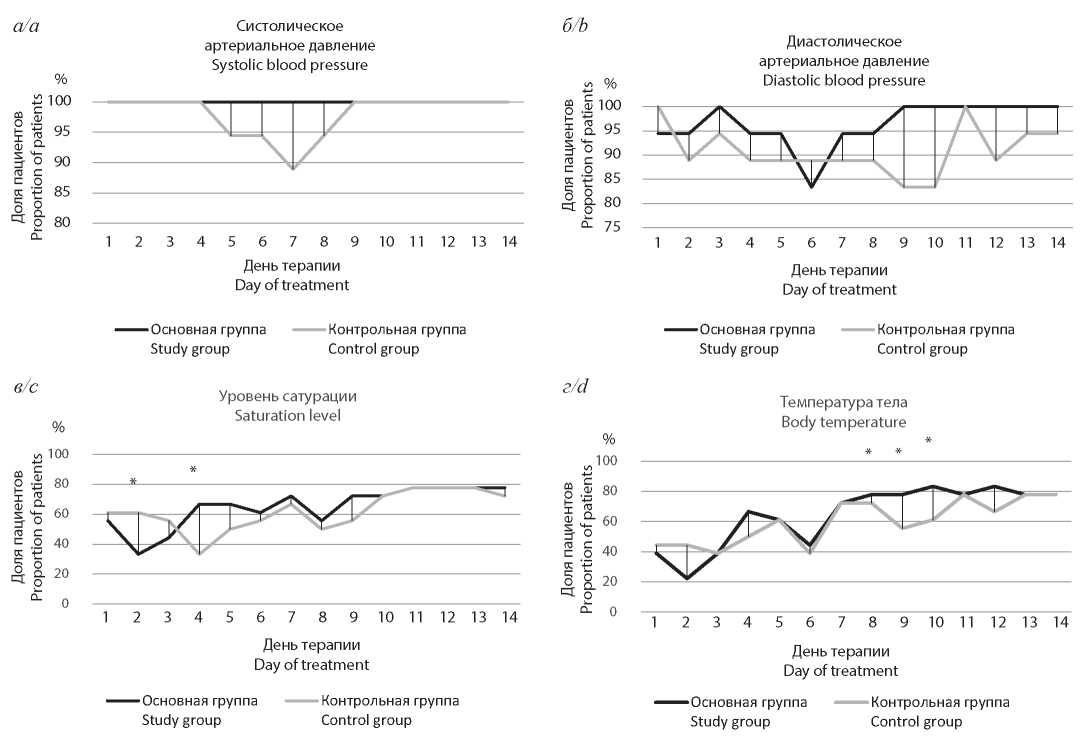
Цель данной работы - оценка влияния ИФН-γ при подкожном введении у лиц с вирусной пневмонией на динамику жизненно важных показателей и длительность госпитализации.
Материал и методы. В открытое рандомизированное малоинтервенционное исследование были включены пациенты старше 18 лет обоих полов с новой коронавирусной инфекцией среднетяжёлого течения. Препарат ИФН-γ назначался по 500 000 МЕ подкожно 1 раз в сутки ежедневно на протяжении 5 дней.
Результаты. Установлена более благоприятная динамика стабилизации жизненно важных показателей в сочетании с сокращением длительности лихорадки и продолжительности госпитализации на 2 сут при применении ИФН-γ в дополнение к комплексной терапии, что позволяет предположить позитивное влияние этого вещества на процессы восстановления больных со среднетяжёлой степенью COVID-19. Особого внимания заслуживает тот факт, что получавшие рекомбинантный ИФН-γ не имели прогрессирования дыхательной недостаточности и не требовали перевода в отделение интенсивной терапии (ОРИТ). Обсуждение. Представленная работа подтверждает полученные ранее данные о положительном влиянии ИФН-γ на скорость клинической стабилизации и выздоровления лиц с внебольничными пневмониями и вирусными инфекциями. Результаты настоящего исследования ограничены небольшим количеством участников и требуют дальнейшего изучения свойств препарата в рамках пострегистрационных исследований.
Заключение. Прогресс в лечении больных среднетяжёлой формой COVID-19 путём дополнения комплексной терапии рекомбинантным ИФН-y может обоснованно расширить ряд существующих методов лечения этой инфекции.
 47-54
47-54


Синтез и характеристика вирусоподобных частиц ротавируса А (Reoviridae: Sedoreovirinae: Rotavirus: Rotavirus A) человека
Аннотация
Введение. Ротавирусная инфекция (РВИ) является основной причиной острого гастроэнтерита у детей до 5 лет. Проблема разработки новых вакцин против ротавируса (РВ) А до настоящего времени актуальна, так как возбудитель имеет множество генотипов, часть из которых представлена только в определённых регионах. Один из перспективных путей создания эффективных и безопасных вакцинных препаратов в настоящее время - использование вирусоподобных частиц (ВпЧ).
Цель данного исследования - разработать технологию получения ВпЧ на основе белков РВ VP4, VP7, генотипы которых наиболее представлены на территории Российской Федерации, а также VP2 и VP6; дать их молекулярно-генетическую и вирусологическую характеристику.
Материал и методы. В работе использовали вирулентный штамм Wa G1P[8] РВ А человека, адаптированный к клеточной культуре MARC-145, который культивировали и очищали по описанной авторами ранее методике. Применяли стандартные молекулярно-генетические и цитологические методы: синтез генов, клонирование в трансферные плазмиды, получение рекомбинантных бакуловирусов; производство ВпЧ с помощью бакуловирусной системы экспрессии Bac-to-Bac в клетках насекомых; центрифугирование в растворе сахарозы; иммуноферментный анализ (ИФА); электронная микроскопия (ЭМ); электрофорез (ЭФ) в полиакриламидном геле с додецилсульфатом (лаурилсульфатом) натрия (ПААГ-ДСН); имму-ноблоттинг.
Результаты. Для включения в состав ВпЧ выбраны 6 наиболее распространённых в России генотипов РВ A по белкам VP4 и VP7 (G1, G2, G4, G9, P4, P8), а также VP2 и VP6. Получены рекомбинантные баку-ловирусы, содержащие оптимизированные для экспрессии в клетках насекомых последовательности выбранных генов. Клетки совки (Trichoplusia ni) коинфицированы различными сочетаниями указанных вирусов с получением ВпЧ, состоящих из 2-4 белков. Эти частицы очищены центрифугированием в растворе сахарозы. По результатам ЭМ морфология и размер частиц соответствовали вириону РВ А. Присутствие в них белков данного патогена подтверждено методами ИФА, электрофореза в ПААГ-ДСН и последующего иммуноблоттинга.
Заключение. Разработана и оптимизирована технология синтеза 3-слойных ВпЧ, состоящих из белков РВ А VP2, VP4, VP6, VP7. Полученные частицы содержат белки VP4 и VP7 6 генотипов, наиболее представленных на территории России, и могут быть использованы для создания вакцинных препаратов против РВ А.
 55-64
55-64


Разработка метода количественного определения вирусной РНК для контроля специфической активности вакцины против геморрагической лихорадки с почечным синдромом
Аннотация
Введение. Геморрагическая лихорадка с почечным синдромом (ГЛПС) занимает ведущее место среди природно-очаговых болезней человека в Российской Федерации. Этиотропная терапия заболевания в настоящее время отсутствует. Наиболее действенным методом контроля этой инфекции может стать вакцинопрофилактика. Основными критериями оценки инактивированной вакцины являются её иммуногенность и специфическая активность.
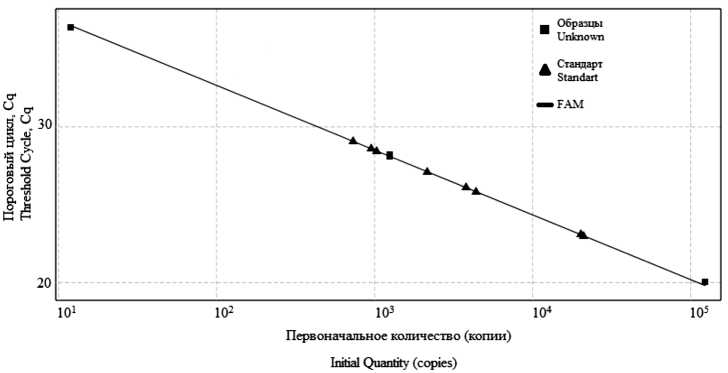
Цель исследования - разработка чувствительной и специфичной методики проведения ПЦР в реальном времени с целью количественного определения вирусной РНК в инактивированной вакцине, а также установление корреляции между содержанием генетического материала вируса и выраженностью иммуногенности. Материал и методы. В качестве диагностической мишени для олигонуклеотидов и флуоресцентных зондов выбраны фрагменты L-сегмента вакцинных штаммов вирусов ГЛПС Пуумала, Хантаан, Сочи. Иммуногенность экспериментальных вакцин контролировали по индукции нейтрализующих антител (нАТ) в ответ на иммунизацию мышей линии BALB/c.
Результаты. Разработана высокоспецифичная, чувствительная методика проведения ПЦР в реальном времени, имеющая высокий показатель воспроизводимости. Аналитическая чувствительность составила для вирусов Пуумала 1,24 ± 1,5 х 102 копий/мл, Хантаан - 1,16 ± 1,4 х 102 копий/мл, Сочи - 1,32 ± 1,8 х 102 копий/мл при содержании вируса 1,5 ± 0,5, 1,8 ± 0,5 и 2,2 ± 0,5 lg ФОЕ/мл соответственно. Показано, что количество вирусной РНК в составе экспериментальных вакцинных препаратов, инактивированных β-про-пиолактоном (β-ПЛ), пропорционально титру нАТ в ответ на иммунизацию.
Обсуждение. Установлено, что способ инактивирования вируса влияет на выявляемое количество копий РНК, не оказывая при этом воздействия на иммуногенность, что указывает на равнозначное повреждение белков-иммуногенов при разной степени повреждения вирусной РНК. Прямая зависимость между содержанием копий нуклеиновой кислоты вируса и иммуногенностью позволяет использовать этот критерий для дозирования вакцинного препарата.
Заключение. Разработанная система оценки количественного содержания вирусной РНК делает перспективным её применение для контроля специфической активности вакцины против ГЛПС.
 65-73
65-73


Течение и исходы хронического вирусного гепатита D у жителей Республики Тыва как эндемичного региона
Аннотация
Введение. Гепатит D (дельта, 5) вызывается РНК-содержащим вирусом (вирус гепатита D, hepatitis D virus -HDV), выделенным в род Deltavirus, и представляет собой наиболее тяжёлое и трудно поддающееся лечению заболевание как среди вирусных гепатитов, так и инфекционных болезней в целом. Развитие HDV-инфекции в организме-хозяине возможно только при наличии вируса гепатита В (HBV). Двойное инфицирование HBV и HDV по сравнению с моноинфекцией первым из них в большей степени связано с ускоренным прогрессированием хронического гепатита, трансформацией его в цирроз печени (ЦП) и неблагоприятным прогнозом. Данные о влиянии клинико-биохимических и вирусологических факторов на профиль инфекционного процесса у больных хроническим вирусным гепатитом (ХВГ) D в настоящее время ограничены в силу недостаточного количества исследований по этой тематике.
Цель работы - определить демографические, клинико-биохимические и вирусологические факторы, влияющие на течение и прогрессирование ХВГ D у наблюдавшихся на протяжении 10 лет пациентов, проживающих на территории одного из эндемичных регионов РФ - Республики Тыва.
Материал и методы. Проанализированы изменения клинико-лабораторных показателей в динамике у 121 инфицированного HDV пациента с различным течением заболевания, находившихся под наблюдением с 2009 по 2019 г. Среди участников выделены 3 группы: 1-я группа - 61 человек с прогрессированием ХВГ до ЦП (класс В-С по Чайлд-Пью), 2-я - 49 больных с непрогрессирующим ХВГ и 3-я - 11 пациентов, имевших медленно прогрессирующий ЦП (класс А). Изучались демографические данные, наличие детектируемой ДНК HBV, показатели функционального состояния печени: активность аланиновой (АЛТ) и аспарагиновой (АСТ) аминотрансфераз, щелочной фосфатазы (ЩФ), гамма-глутамилтранспептидазы (гамма-глу-тамилтрансферазы) (ГГТП) и содержание общего билирубина (ОБ). Степень выраженности печёночной энцефалопатии (ПЭ) оценивали по длительности выполнения теста связи чисел (ТСЧ).
Результаты. Все исследуемые принадлежали к одной этнической группе (тувинцы), были инфицированы HDV с одинаковым генотипом и сохраняли положительную РНК HDV на протяжении всего периода наблюдения. Достоверные различия по гендерному соотношению и среднему возрасту на момент включения в исследование между группами отмечены не были. В 1-й группе среднее количество лет от начала наблюдения до формирования ЦП составило 3,65 ± 2,3 года, до летального исхода - 4,5 ± 3,0 года. Достоверно более высокие значения активности АСТ, ЩФ, ГГТП, содержания ОБ и длительности выполнения ТСЧ выявлены в 1-й группе по сравнению со 2-й; показатели активности АЛТ в них значимо не различались. При сравнении участников с прогрессированием заболевания и медленно прогрессирующим ЦП (1-я и 3-я группы) не выявлено статистически достоверных различий ни по одному из клинико-биохимических параметров. Показатели активности АЛТ, ГГТП, уровня ОБ и выполнения ТСЧ были достоверно выше у страдавших медленно прогрессирующим ЦП (3-я группа) по сравнению со 2-й группой; различия по активности АСТ и ЩФ между ними не выявлены. Положительный результат обнаружения ДНК HBV достоверно чаще отмечен у имевших прогрессирующее течение болезни и у пациентов с ХВГ, чем у больных с медленно прогрессирующим ЦП. Не было значимых различий в частоте выявления этого маркёра у исследуемых 1-й и 2-й групп.
Заключение. Полученные на относительно однородной выборке результаты показали, что возраст и пол не являются факторами, влияющими на прогрессирование ХВГ D в ЦП; отсутствие детектируемой ДНК HBV связано с медленным прогрессированием последнего. Выявленные различия клинико-биохимических параметров отражают степень функционального поражения печени при ХВГ D и HDV-ассоциированном циррозе.
 74-83
74-83


РЕЦЕНЗИИ
 84
84