Том 65, № 4 (2020)
- Год: 2020
- Выпуск опубликован: 17.09.2020
- Статей: 6
- URL: https://virusjour.crie.ru/jour/issue/view/45
Весь выпуск
ОБЗОРЫ
Перспектива создания специфических противогриппозных препаратов на основе синтетических малых интерферирующих РНК
Аннотация
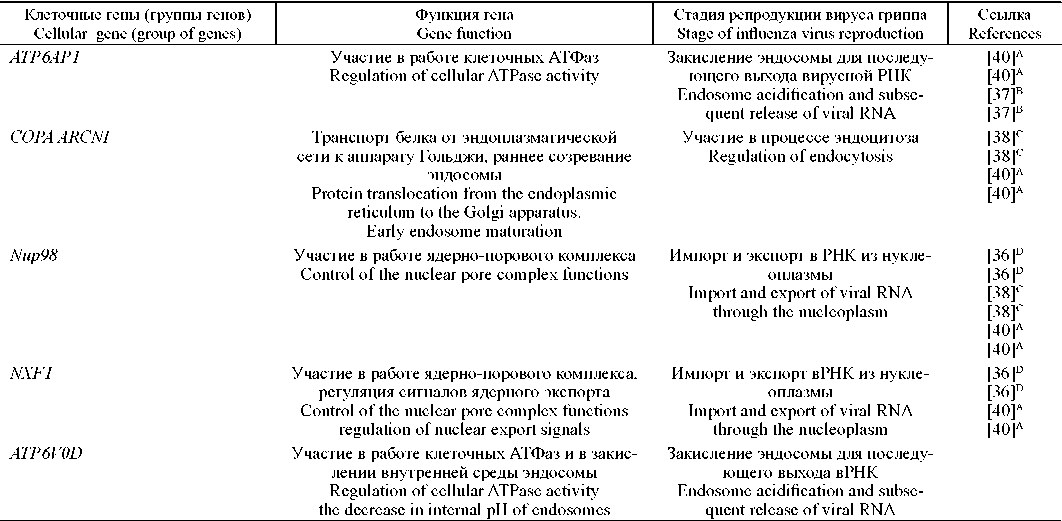
Грипп является одной из самых актуальных проблем здравоохранения во всём мире. Ежегодно гриппом болеют до 15% населения земли, из них около 500 тыс. человек умирают. Особую клиническую значимость представляют вирусы гриппа А и В, имеющие высокий эпидемический и пандемический потенциал. Помимо поражения дыхательных путей, грипп способен вызвать осложнения со стороны сердечно-сосудистой и центральной нервной системы. Несмотря на широкий спектр специфически направленных на различные стадии вирусной репродукции противогриппозных препаратов, наиболее остро стоит проблема формирования вирусной резистентности к традиционным лекарственным препаратам, что требует поиска новых технологий для её преодоления. Перспективным представляется создание лекарственных препаратов, действие которых основано на ингибировании активности вирусных или клеточных генов под влиянием механизмов РНК-интерференции. РНК-интерференция - это каскад регуляторных реакций в эукариотических клетках, вызванный чужеродной экзогенной двухцепочечной РНК, в результате чего происходит расщепление целевой матричной РНК. В настоящем обзоре рассматриваются использование механизма РНК-интер-ференции при разработке специфически направленных противогриппозных средств, а также перспективы, преимущества и недостатки данного подхода. Необходимо учитывать, что важным фактором, снижающим эффективность РНК-интерференции, является формирование резистентности вирусов к действию малых интерферирующих РНК, направленных к вирусным генам. Ввиду этого для преодоления лекарственной устойчивости вируса гриппа наиболее пристального внимания заслуживает исследование применения малых интерферирующих РНК, направленных непосредственно к факторам клетки-хозяина, которые необходимы для репродукции вируса гриппа.
 182-190
182-190


Вирус Эпштейна-Барр (Herpesviridae: Gammaherpesvirinae: Lymphocryptovirus: Human gammaherpesvirus 4): репликативные стратегии
Аннотация
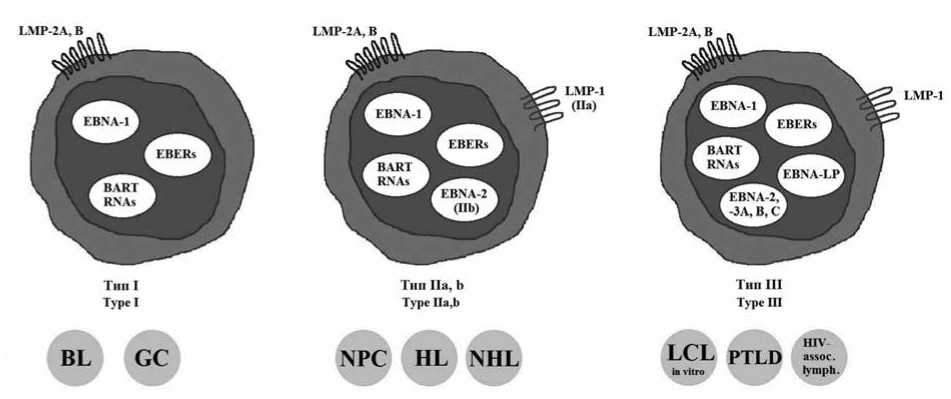
Вирус Эпштейна-Барр (ВЭБ) - один из наиболее распространённых в человеческой популяции, он способен на протяжении всей жизни персистировать в покоящихся В-клетках памяти, в Т-клетках (ВЭБ 2-го типа) и в некоторых недифференцированных эпителиальных клетках. У большинства людей персистенция ВЭБ не сопровождается значительными симптомами, но при частых активациях вируса возрастают риски тяжёлых сопутствующих заболеваний, включая хроническую активную ВЭБ-инфекцию, гемофагоцитарный лимфогистиоцитоз, рассеянный склероз, системную красную волчанку, карциному желудка и носоглотки, а также различные Т- и В-клеточные лимфомы. Большой интерес представляют молекулярные вирусные и клеточные процессы во время бессимптомной или малосимптомной персистенции ВЭБ. В этом обзоре рассматриваются поведение вирусной ДНК в заражённой клетке, формы её существования (линейная, циркулярная эписома, хромосомно-интегрированная форма), а также методы копирования генома ВЭБ. Рассмотрены два тесно связанных цикла вируса - литический и латентный. Литическая активация неблагоприятна для выживания конкретного вирусного генома в клетке, она запускается в результате дифференцировки латентно инфицированной клетки или появления стресс-сигналов из-за неблагоприятных условий внеклеточной среды. ВЭБ обладает большим количеством адаптивных механизмов для предотвращения литической реактивации и снижения враждебности иммунных клеток хозяина. Понимание молекулярных аспектов персистенции ВЭБ поможет в будущем разработать более эффективные, таргетные препараты для лечения как самой вирусной инфекции, так и сопутствующих заболеваний.
 191-202
191-202


ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
Закономерности эпидемического распространения SARS-CoV-2 в условиях мегаполиса
Аннотация
Цель исследования - изучить закономерности, свойственные эпидемическому процессу COVID-19, в условиях мегаполиса, в фазах подъёма, стабилизации и снижения заболеваемости, а также оценить эффективность противоэпидемических мероприятий.
Материал и методы. Проведено комплексное изучение распространения SARS-CoV-2 в Москве с использованием эпидемиологического, молекулярно-генетического и статистического методов исследования в период пандемии COVID-19.
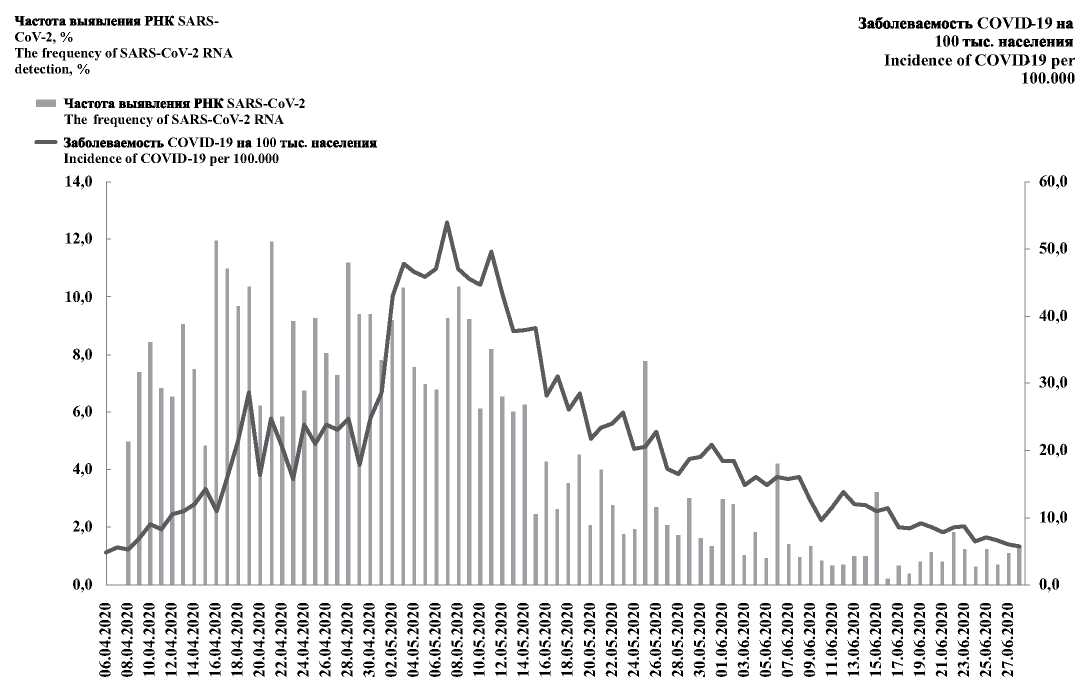
Результаты и обсуждение. Показано, что применение максимально жёстких организационно-ограничительных мер в масштабах Москвы, обеспечивающих разрыв механизма передачи SARS-CoV-2, и высокая дисциплина населения по исполнению режима самоизоляции позволили не допустить экспоненциального роста заболеваемости COVID-19. Анализ динамики выявления новых случаев COVID-19 показал, что эффект от применения мер по разобщению и режима самоизоляции в условиях мегаполиса наступает через временной промежуток, равный 3,5 инкубационного периода, при его максимальной длительности 14 дней. Установлено, что показатель частоты определения РНК SARS-CoV-2 среди условно здорового населения и его динамика - важные параметры мониторинга, особенно на фазах роста и стабилизации заболеваемости COVID-19, позволяющие в перспективе 1-2 инкубационных периодов (14-28 дней) прогнозировать развитие эпидемиологической ситуации. Общий коэффициент летальности, рассчитанный за период наблюдения (06.03.2020-23.06.2020) в Москве, составил 1,73%.
Заключение. В результате проведённого эпидемиологического анализа ситуации с COVID-19 в Москве определены некоторые закономерности распространения SARS-CoV-2 и оценена эффективность противоэпидемических мероприятий, направленных на разрыв механизма передачи возбудителя.
 203-211
203-211


Разработка инактивированной культуральной вакцины против жёлтой лихорадки
Аннотация
Введение. Жёлтая лихорадка (ЖЛ) - одно из самых распространённых вирусных заболеваний человека. Единственная на сегодняшний день доступная живая вакцина против ЖЛ на основе куриных эмбрионов, инфицированных аттенуированным штаммом 17D вируса ЖЛ, относится к наиболее эффективным вакцинным препаратам. Однако живая вакцина ассоциирована с тяжёлыми поствакцинальными осложнениями, в том числе с висцеротропным синдромом (примерно 0,4 случая на 100 тыс. вакцинированных). В связи с этим разработка и внедрение высокоочищенной инактивированной вакцины против ЖЛ призвана обеспечить максимальную безопасность вакцинации.
Цель исследования - разработка и оценка иммуногенности культуральной инактивированной вакцины против ЖЛ на уровне лабораторной модели.
Материал и методы. В ходе исследования проведены адаптация штамма 17D вируса ЖЛ к культуре клеток Vero, культивирование, удаление клеточной ДНК, инактивация β-пропиолактоном, концентрирование, хроматографическая очистка, определение белка и антигена вируса ЖЛ, оценка иммуногенности на мышах параллельно с коммерческой живой вакциной.
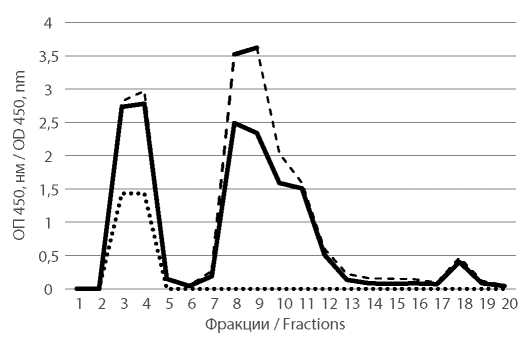
Результаты и обсуждение. Определение специфических антител класса G (IgG) и вируснейтрализующих антител в сыворотках крови иммунизированных мышей показало высокий уровень антител, превышающий таковой при иммунизации коммерческой живой вакциной. Оптимальная доза антигена в вакцине по общему белку составила 50 мкг/мл (5 мкг/0,1 мл - доза и объём на 1 вакцинацию мышей). Таким образом, лабораторный вариант культуральной инактивированной вакцины против ЖЛ по эффективности не уступает коммерческой живой вакцине и даже превосходит её.
Заключение. Разработан лабораторный вариант культуральной инактивированной вакцины против ЖЛ, не уступающий по иммуногенности (на модели животных) коммерческой живой вакцине.
 212-217
212-217


Серопревалентность вируса гепатита Е (Hepeviridae: Orthohepevirus: Orthohepevirus A) среди беременных женщин в эндемичном регионе Кыргызстана
Аннотация
Введение. Гепатит E (ГЕ) является важной проблемой общественного здравоохранения во всём мире, и особенно опасен для беременных, среди которых летальность достигает 25%. Распространение серомаркеров ГЕ среди беременных в эндемичных регионах стран Центральной Азии мало изучено.
Цель исследования - изучение серопревалентности вируса гепатита Е (ВГЕ) среди беременных в регионе Кыргызстана с повышенной заболеваемостью ГЕ.
Материал и методы. Сыворотки крови беременных, полученные из лечебно-профилактических учреждений Бишкека, Оша и Ошской области с сентября 2016 г. по октябрь 2019 г., и здоровых небеременных женщин группы сравнения тестировали с помощью тест-систем «ДС-ИФА-АНТИ-HEV-G» и «ДС-ИФА-АНТИ-HEV-М» (НПО «Диагностические системы», Россия).
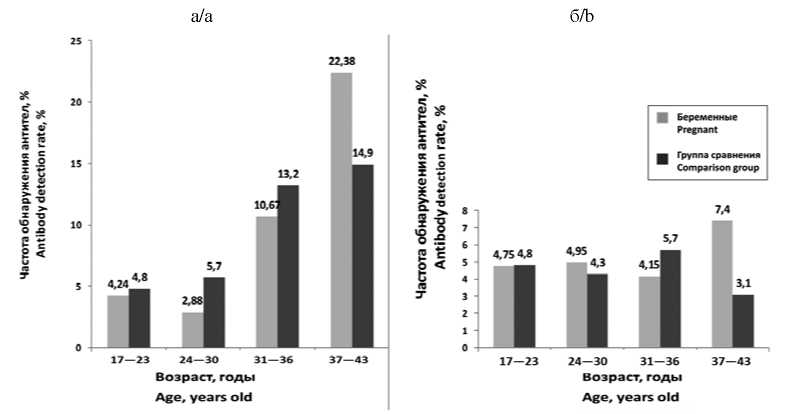
Результаты. IgG-антитела к ВГЕ выявлены у 87 (5,9%) из 1472 обследованных беременных, 1дМ-антитела - у 64 (4,8%) из 1378; 5 (0,34%) проб были одновременно позитивны по IgG- и IgM-антителам. Антитела к ВГЕ у женщин трёх возрастных категорий от 17 до 36 лет исследуемой группы и группы сравнения выявлялись со схожими значениями частоты. Изучение сезонной динамики серопревалентности ВГЕ у беременных с февраля по сентябрь 2019 г. показало тенденцию к повышению коэффициента позитивности специфических IgM-антител к началу осени. Антитела к ВГЕ чаще выявлялись у жительниц Ошской области.
Заключение. Показан высокий риск инфицирования ВГЕ беременных в обследованном регионе Кыргызстана.
 218-227
218-227


В ПОМОЩЬ ВИРУСОЛОГУ
Изучение противовирусной активности жидких сред для хранения роговицы в отношении вируса простого герпеса in vitro
Аннотация
Цель исследования - изучить противовирусную активность 7 образцов жидкой среды для хранения роговицы на модели герпесвирусной инфекции in vitro.
Материал и методы. Изучена противовирусная активность 7 образцов жидкой среды для хранения роговицы (ОСХР) на модели герпесвирусной инфекции, обусловленной вирусом простого герпеса 1-го типа (ВПГ-1), штамм ЕС, в культуре клеток Vero с использованием вирусологического и статистического методов исследования.
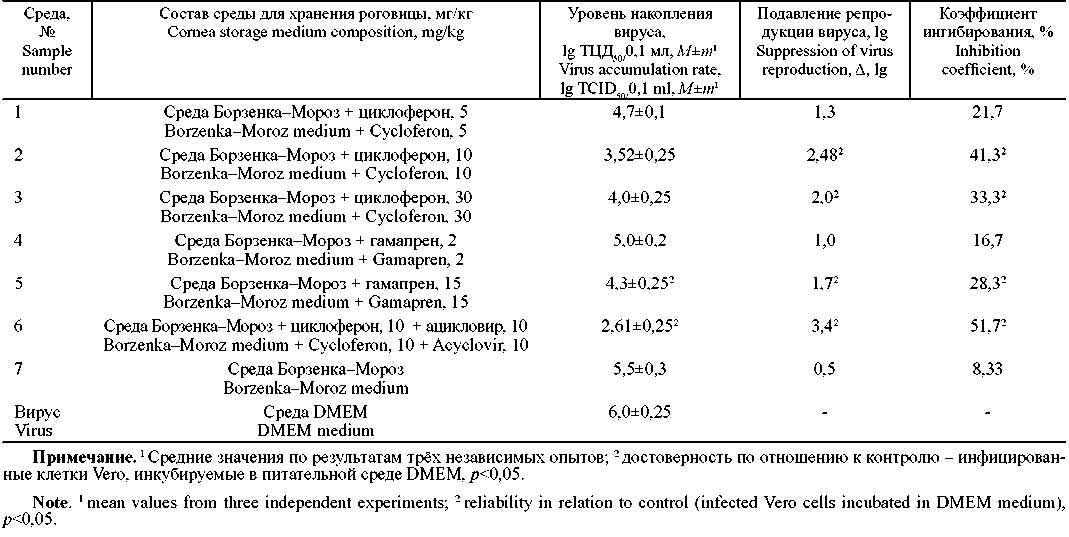
Результаты и обсуждение. Показано, что все исследуемые образцы среды для хранения роговицы, в том числе и базовая среда Борзенка-Мороз, не оказывают цитотоксического действия на культуру клеток Vero. Установлено, что 4 из 7 образцов жидкой среды для хранения роговицы обладают достоверной противовирусной активностью в отношении ВПГ-1 при использовании по терапевтической (через 1 ч после инфицирования) и по профилактической (за 2 ч до инфицирования) схемам. Противовирусная активность установлена у 2 образцов, содержащих индуктор интерферона циклоферон в концентрации 10 и 30 мг/кг (ОСХР 2, 3 соответственно); у образца, содержащего индуктор интерферона гамапрен 15 мг/кг (ОСХР 5), и у образца, содержащего комбинацию препаратов: циклоферон 10 мг/кг и ациклический аналог нуклеозида - ацикловир 10 мг/кг (ОСХР 6). Максимальный статистически достоверный ингибиторный эффект по отношению к ВПГ-1 по результатам двух схем испытаний был выявлен у ОСХР 6, содержащего комбинацию препаратов. На фоне его применения инфекционная активность тест-вируса снижалась в среднем на 3,2 lg, коэффициент ингибиции составил 54,5%.
Заключение. Результаты исследования свидетельствуют о перспективности использования образцов противовирусных сред для хранения донорских роговиц (образцы 2, 3, 5 и 6) с целью повышения эффективности кератопластики у больных офтальмогерпесом.
 228-236
228-236