Эпидемический сезон 2023–2024 гг.: палитра возбудителей ОРВИ на некоторых территориях РФ и в регионах ВОЗ
- Авторы: Бурцева Е.И.1, Бреслав Н.В.1, Мукашева Е.А.1, Краснослободцев К.Г.1, Кириллова Е.С.1, Трушакова С.В.1, Комарова И.А.2, Феодоритова Е.Л.1, Панова А.Д.1, Кистенева Л.Б.1, Хлопова И.Н.1, Кружкова И.С.1, Крепкая А.С.1, Морозова Е.О.1, Игнатьева А.В.1, Комиссаров А.Б.3, Тюрин И.Н.4, Самков А.А.4, Антипят Н.А.4
-
Учреждения:
- ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
- ФГБОУ ВО «Тихоокеанский государственный медицинский университет» Минздрава России
- ФГБУ «Научно-исследовательский институт гриппа им. А.А. Смородинцева» Минздрава России
- ГБУЗ «Инфекционная клиническая больница № 1» Департамента здравоохранения города Москвы
- Выпуск: Том 70, № 3 (2025)
- Страницы: 234-245
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://virusjour.crie.ru/jour/article/view/16716
- DOI: https://doi.org/10.36233/0507-4088-302
- EDN: https://elibrary.ru/MQXOMB
- ID: 16716
Цитировать
Аннотация
Цель настоящей работы заключалась в определении особенностей циркуляции возбудителей острых респираторных вирусных инфекций (ОРВИ), в том числе вирусов гриппа и SARS-CoV-2, в период эпидемического сезона 2023–2024 гг. в регионах Всемирной организации здравоохранения (ВОЗ) и ряде регионов РФ.
Материалы и методы. В статье использованы вирусологические, иммунологические и статистические методы, а также аналитический материал сайта ВОЗ для оценки особенностей циркуляции возбудителей ОРВИ в регионах ВОЗ и на отдельных территориях РФ.
Результаты и обсуждение. Частота выявления положительных проб в клинических материалах составила: вирусов гриппа 7,7%, ОРВИ – 17,1% и SARS-CoV-2 – 6,5%. По антигенным и молекулярно-генетическим свойствам популяция доминирующего подтипа вируса гриппа A(H3N2) была гетерогенной и отличалась от вакцинного штамма. Сохранен благоприятный профиль чувствительности эпидемических штаммов к препаратам с антинейраминидазной активностью (осельтамивиру и к занамивиру) и ингибитору кэп-зависимой эндонуклеазы (балоксавиру марбоксилу). Отмечена тенденция к росту активности таких респираторных патогенов, как: HPIV, HAdV, HRsV, HRV, HCoV и HMPV. Экспертами ВОЗ выработаны рекомендации по составу гриппозных вакцин для стран Северного и Южного полушарий с заменой компонента вируса гриппа A(H3N2): А/Дарвин/9/2021 на A/Таиланд/8/2022 и А/Хорватия/10136RV/2023 соответственно. Продолжают регистрировать случаи инфицирования людей вирусами гриппа птиц и свиней.
Заключение. На фоне относительно низкой циркуляции новых вариантов SARS-CoV-2 в сезоне 2023-2024гг., в странах Северного полушария регистрировали эпидемическую активность вирусов гриппа в традиционные сроки. В глобальном масштабе его начало было связано с вирусом гриппа A(H3N2), затем регистрировали рост активности вируса гриппа A(H1N1) pdm09 и гриппа В. Прослежены, как и в предыдущие сезоны, различия по долевому участию вирусов гриппа в регионах ВОЗ, в том числе, и по городам РФ.
Полный текст
Введение
На фоне продолжающейся циркуляции нового коронавируса SARS-CoV-2 активность других респираторных патогенов, в том числе гриппа, в течение последних 3 эпидемических сезонов (2020–2023 гг.) была ниже по сравнению с предпандемическим по COVID-19 периодом [1–4]. Несмотря на это, была отмечена изменчивость популяций вирусов SARS-CoV-2 и гриппа, что не могло не повлиять на особенности эпидемического процесса острых респираторных вирусных инфекций (ОРВИ) в постковидный период1 [5, 6]. Изучение особенностей изменчивости вирусных патогенов, а также способность к прогнозированию эволюционных связей может повысить уровень контроля над возбудителями ОРВИ и, в первую очередь, вирусами гриппа и SARS-CoV-2, в отношении которых разработаны вакцины [7]. При продолжении ранее проводимых ежегодных исследований определенный интерес представляла оценка особенностей развития эпидемии гриппа 2023–2024 гг. по частоте встречаемости и спектру респираторных патогенов на отдельных территориях РФ, а также в регионах Всемирной организации здравоохранения (ВОЗ). Очевидной является необходимость анализа результатов изучения эволюционной изменчивости вирусов гриппа птиц и свиней, случаи которых были детектированы у людей в разных странах мира, для оценки рисков преодоления межвидового барьера и возможного формирования нового пандемического варианта2.
Цель настоящей работы заключалась в определении особенностей циркуляции возбудителей ОРВИ, в том числе вирусов гриппа и SARS-CoV-2, в период эпидемического сезона 2023–2024 гг. в ряде регионов РФ и ВОЗ.
Материалы и методы
Сбор данных по заболеваемости и лабораторной диагностике возбудителей ОРВИ. В рамках осуществления эпидемиологического надзора за циркуляцией вирусов гриппа и ОРВИ в РФ Центр экологии и эпидемиологии гриппа (ЦЭЭГ) Института вирусологии им. Д.И. Ивановского ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России в сотрудничестве с 10 опорными базами, представленными территориальными управлениями и ФБУЗ «Центры гигиены и эпидемиологии» Роспотребнадзора в Европейской части (гг. Новгород Великий, Липецк, Владимир, Ярославль, Пенза, Чебоксары), на Урале (г. Оренбург), Сибири (г. Томск) и Дальнем Востоке (гг. Биробиджан и Владивосток), провели анализ показателей заболеваемости и госпитализации в разных возрастных группах населения, а также результатов лабораторной диагностики респираторных патогенов. Период наблюдения ‒ с 40-й недели (октябрь) 2023 г. по 39-ю неделю (сентябрь) 2024 г.
Анализ заболеваемости гриппом и ОРВИ в разных возрастных группах, изоляция вирусов гриппа, постановка полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР), реакции торможения гемагглютинации, оценка чувствительности к противогриппозным препаратам, а также статистическая обработка полученных результатов описаны ранее [1, 2]. В рамках традиционного надзора объем исследований с помощью лабораторных методов составил: для вирусов гриппа – 44 719 клинических образцов/изолятов/штаммов, ОРВИ – 40 277 клинических образцов и SARS-CoV-2 – 30 890 клинических образцов.
Полногеномная амплификация вирусов гриппа А и B была проведена по ранее описанной методике [8, 9]. Библиотека комплементарной ДНК была приготовлена с использованием набора SQK-LSK109 (Oxford Nanopore, Великобритания) с последующим секвенированием на приборе MinION (Oxford Nanopore, Великобритания). Биоинформационная обработка данных проведена с использованием пакетов программного обеспечения guppy вер.6.3.8, porechop вер.0.2.4, nanofilt вер.2.3.0, minimap2 вер.2.24, medaka вер.1.7.2 и bcftools вер.1.13.
Этическое утверждение. Исследование проводилось при добровольном информированном согласии пациентов. Протокол исследования одобрен Этическим комитетом ГБУЗ г. Москвы «Инфекционная клиническая больница № 1 Департамента здравоохранения города Москвы» (Протокол № 8 от 28.12.2022).
Результаты
В период с октября 2023 г. (40-я неделя) по сентябрь 2024 г. (39-я неделя) на сотрудничающих с ЦЭЭГ территориях превышение эпидемического порога заболеваемости ОРВИ по отношению к среднему показателю по РФ (72,6 на 10 тыс. населения) регистрировали в периоды 47–52-й недели 2023 г., 2–7-й недели, 9-й и 11-й недели 2024 г. Максимальную заболеваемость по совокупному населению (среднее значение по данным 10 городов РФ) регистрировали на 51-й неделе 2023 г. (135,9) – в те же сроки, что и в предыдущем сезоне, но с более низким показателем (157,0). В этот период частота положительных проб на респираторные патогены составила 34,2%, в том числе вирусы гриппа – 18,9%, SARS-CoV-2 – 5,7%, другие ОРВИ – 9,6%.
Средний показатель заболеваемости ОРВИ за весь сезон был незначительно ниже по сравнению с показателем предыдущего периода (69,1 и 71,6 соответственно); в то же время отмечали незначительный рост показателя у детей 0–2 лет (среднее 303,1 с интервалом 6,9–553,8 и 294,4 (9,2–475,2) соответственно); в других возрастных группах отмечено снижение: у детей 3–6 лет (264 (6,4–409,6) и 273,9 (10,5–425,4) соответственно), школьников (137,6 (5,5–225,6) и 141,4 (9,4–218,3) соответственно) и взрослых (41,6 (29,0–58,3) и 43,6 (19,4–54,3) соответственно).
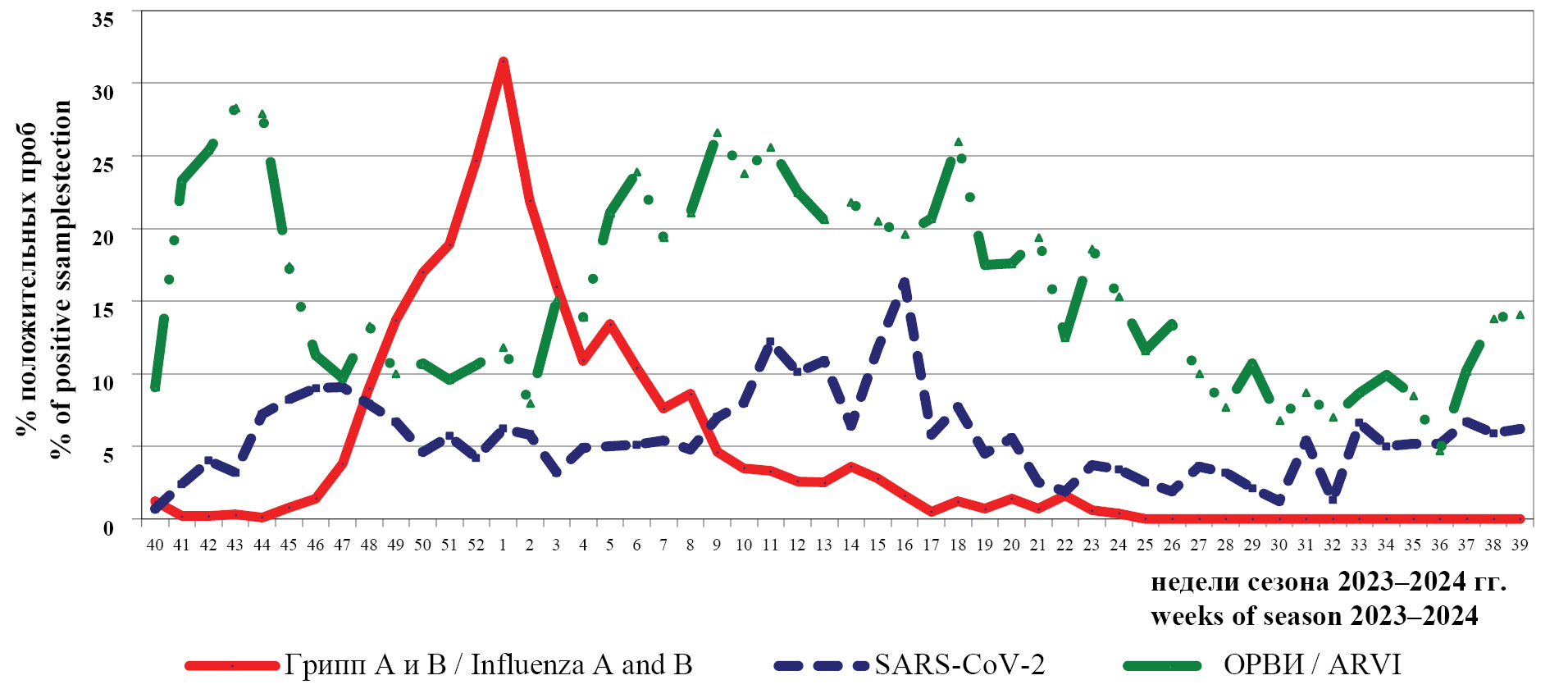
Динамика частоты положительных находок для вирусов гриппа А и В, SARS-CoV-2 и ОРВИ (в том числе: вирусы парагриппа 1, 2, 3 и 4-го типов (human Parainfluenza virus-1–4, HPIV); аденовирусы групп B, C и E ((human Adenovirus B, C, E, HAdV); респираторно-синцитиальный вирус (human Respiratory Syncytial virus, HRsV); риновирус (human Rhinovirus, HRV); бокавирус (human Bocavirus, HBoV); метапневмовирус человека (human Metapneumovirus, HMPV); коронавирус (human Coronavirus, HCoV)) методом ОТ-ПЦР в период октября 2023 г. – сентября 2024 г. представлена на рис. 1.
Рис. 1. Динамика частоты выявления положительных образцов на вирусные респираторные возбудители (%) в клинических материалах методом ОТ-ПЦР в период эпидемического сезона 2023–2024 гг.
Fig. 1. Dynamics of the frequency of detection of positive samples for virus respiratory pathogens (%) in clinical samples by RT-PCR during epidemic season 2023–2024.
Эпидемический сезон 2023–2024 гг., как и предыдущий, стартовал с высоких показателей частоты положительных проб на ОРВИ негриппозной этиологии (28,3%). На фоне снижающейся активности патогенов ОРВИ и относительно «невысокой» частоты выявления положительных проб на SARS-CoV-2 (до 9,1%) был отмечен рост активности вирусов гриппа с максимальными показателями числа положительных проб (31,5%) в период 1-й недели 2024 г. Эти данные указывают на высокую эпидемическую активность вирусов гриппа в этот период и коррелируют с показателями заболеваемости ОРВИ.
В период 3–24-й недели 2024 г. регистрировали рост активности других респираторных патогенов с максимальными показателями частоты положительных проб до 26,0%; и вплоть до 27-й недели 2024 г. частота выявления положительных проб была не менее 10,0%. Рост показателей был отмечен также в период 37–39-й недели 2024 г. (до 14,1%).
Наибольшая активность SARS-CoV-2 была прослежена в период 11–16-й недели 2024 г.
Частота положительных находок по результатам ПЦР в период 40-й недели 2023 г. – 26-й недели 2024 г. составила: для гриппа – 7,7% (из 38 070 обследованных), ОРВИ – 17,1% (из 33 869 обследованных) и SARS-CoV-2 – 6,5% (из 26 257 обследованных); в период июня–сентября 2024 г. (27–39-я неделя 2024 г.) показатели были значительно ниже и составили: для ОРВИ – 9,7% (из 6408 обследованных) и SARS-CoV-2 – 4,9% (из 4633 обследованных). При этом их активность различалась в разных городах РФ (табл. 1).
Таблица 1. Результаты ПЦР-диагностики гриппа, SARS-CoV-2 и некоторых ОРВИ в период октября 2023 г. – сентября 2024 г. в ЦЭЭГ НИЦЭМ им. Н.Ф. Гамалеи и на сотрудничающих с ним территориях РФ
Table 1. The results of PCR diagnostics of influenza, SARS-CoV-2 and some acute respiratory infections in the period October 2023 – September 2024 at the Centre of Ecology and Epidemiology of Influenza (CEEI) in National Research Centre of N.F. Gamaleya and in the territories of the Russian Federation cooperating with it
Центры гигиены и эпидемиологии городов, областей, республик Canters of Hygiene and Epidemiology of cities, regions, republics | Число образцов, изученных на наличие респираторных патогенов методом ОТ-ПЦР The number of samples examined for the presence of respiratory pathogens by RT-PCR | |||||||||||
грипп influenza viruses | ОРВИ, сезонные acute respiratory infections, seasonal | SARS-CoV-2 | ||||||||||
число образцов number of samples | % «+» | число образцов number of samples | HPIV % «+» | HAdV % «+» | HRsV % «+» | HRV % «+» | HCoV % «+» | HBoV % «+» | HMPV % «+» | число образцов number of samples | % «+» | |
ЦЭЭГ, Москва CEEI, Moscow | 1404 | 13,8 | 595 | 1,5 | 3,4 | 2,7 | 12,9 | 3,7 | 0,2 | 2,0 | 1404 | 13,6 |
Вел. Новгород Vel. Novgorod | 1222 | 1,8 | 1024 | 0,7 | 0 | 2,3 | 0 | 0 | 0 | 0 | 0 | 0 |
Липецк Lipetsk | 4117 | 1,5 | 4117 | 0,5 | 0,3 | 0,3 | 0,5 | 0,4 | 0,6 | 4117 | 0,8 | |
Владимир Vladimir | 2330 | 5,7 | 1663 | 2,4 | 1,3 | 5,5 | 6,8 | 2,1 | 2,4 | 2,2 | 2234 | 3,2 |
Ярославль Yaroslavl | 6196 | 8,5 | 4159 | 1,7 | 2,3 | 2,7 | 8,3 | 3,9 | 1,0 | 4,1 | 4587 | 8,2 |
Пенза Penza | 4058 | 4,2 | 3549 | 1,1 | 1,6 | 2,3 | 5,0 | 1,1 | 0,4 | 0,5 | 3549 | 1,3 |
Чебоксары Cheboksary | 3348 | 6,2 | 3348 | 0,7 | 0,6 | 0,9 | 0,03 | 1,6 | 0 | 0 | 3422 | 10,0 |
Оренбург Orenburg | 10 817 | 1,7 | 10 817 | 1,5 | 1,0 | 2,1 | 4,6 | 1,5 | 0,8 | 2,6 | 0 | 0 |
Томск Tomsk | 3265 | 12,9 | 3254 | 1,32 | 1,5 | 2,9 | 8,8 | 2,1 | 0,8 | 1,2 | 3265 | 6,3 |
Владивосток Vladivostok | 5345 | 13,1 | 5345 | 1,9 | 1,8 | 4,7 | 10,5 | 4,0 | 1,0 | 3,1 | 5345 | 8,3 |
Биробиджан Birobidzhan | 2617 | 12,7 | 2406 | 2,9 | 2,5 | 1,1 | 12,6 | 4,2 | 0,9 | 2,5 | 2967 | 8,0 |
Всего Total | 44 719 | 6,6 | 40 277 | 1,5 | 1,3 | 2,4 | 5,9 | 2,1 | 0,8 | 2,0 | 30 890 | 6,3 |
Наиболее высокая частота выявления положительных проб на грипп была отмечена в гг. Москве, Владивостоке, Томске и Биробиджане; SARS-CoV-2 – в гг. Москве, Чебоксарах, Владивостоке и Ярославле. Тройку «лидеров» в структуре сезонных ОРВИ составили HRV (5,9%), HRsV (2,4%) и HCoV (2,1%), при этом более высокие показатели положительных проб на HPIV выявляли в гг. Биробиджане, Владимире и Ярославле; на HAdV – в гг. Москве, Биробиджане и Ярославле; HRV – в гг. Москве, Биробиджане и Владивостоке; HCoV – в гг. Ярославле, Москве и Владимире; HBoV – в гг. Владимире, Владивостоке и Биробиджане; HMPV – в гг. Ярославле, Оренбурге и Биробиджане.
В то же время регионы России не различались по долевому участию типов/подтипов вирусов гриппа (рис. 2). Вирус гриппа A доминировал в сезоне 2023–2024 гг. на всех территориях, сотрудничающих с ЦЭЭГ НИЦЭМ. В структуре вируса гриппа А большую активность проявил A(H3N2), долевое участие которого составило 95,0%. Штаммы вируса гриппа В выявляли только в 5,0% случаев, при этом в отдельных городах его активность была выше по сравнению с другими городами Европейской части РФ: в гг. Москве (10,3%), Липецке (15,3%), Владимире (7,5%), Ярославле (5,5%) и Владивостоке (8,7%).
Рис. 2. Долевое участие вирусов гриппа в период эпидемического сезона 2023–2024 гг. в разных регионах РФ (по данным Центров гигиены и эпидемиологии городов, областей, республик).
Fig. 2. The share of influenza viruses during the epidemic season 2023–2024 in different regions of the Russian Federation (according to the Centers of Hygiene and Epidemiology of cities, regions, republics).
Результаты антигенной характеристики эпидемических штаммов представлены в табл. 2. Исследования проводили в отношении вирусов гриппа, вошедших в состав вакцин в сезоне 2023–2024 гг. для стран Северного полушария3.
Таблица 2. Антигенные свойства эпидемических штаммов вирусов гриппа А и В, выделенных в эпидемическом сезоне 2023–2024 гг.
Table 2. Antigenic properties of epidemic strains of influenza A and B viruses isolated in the epidemic season 2023–2024
Тип/подтип вируса гриппа Type/subtype of the influenza virus | Штаммы вирусов гриппа, вошедшие в состав гриппозных вакцин в сезоне 2023–2024 гг. (отношение к гомологичному титру) Influenza virus strains included in influenza vaccines in the 2023–2024 season (relation to homologous titer) | Число штаммов, близкородственных эталонной сыворотке/число изученных The number of strains closely related to the reference serum/the number of studied | Общее число изученных штаммов The total number of strains studied |
А(H1N1)pdm09 | А/Виктория/4897/22 A/Victoria/4897/22 (1–1/2 : 1/4) | 2 (100%) : 0 | 2 |
Дрейф-вариант Drift variant (< 1/4) | 0 | ||
А(H3N2) | А/Дарвин/9/21 A/Darwin/9/21 (1–1/2 : 1/4) | 52 (27,8%) : 103 (55,1,0%) | 187 |
Дрейф-вариант Drift variant (< 1/4) | 32 (17,1%) | ||
В | Линия Виктория-подобных Victoria-like lineage В/Австрия/135941/21(D3) (1–1/2) B/Austria/135941/21 | 0 : 6 (46,2%) | 13 |
Линия Виктория-подобных Victoria-like lineage Дрейф-вариант Drift variant (< 1/4) | 7 (53,8%) |
В рассматриваемый период со спектром специфических референс-сывороток были изучены антигенные свойства 202 гемагглютинирующих изолятов, выделенных в гг. Москве, Великом Новгороде, Ярославле, Томске, Оренбурге, Биробиджане и Владивостоке: 187 изолятов проявили родство к вирусу гриппа A(H3N2), причем 17,1% из них представляли собой дрейф-варианты и взаимодействовали с сывороткой к вакцинному вирусу A/Дарвин/9/21(H3N2) до 1/8 и ниже гомологичного титра; два изолята проявили близкое родство с вирусом гриппа A(H1N1)pdm09; 13 изолятов, имели родство к вирусу гриппа В и взаимодействовали с сывороткой к вакцинному вирусу В/Австрия/1359417/21 от 1/16 до 1/4 гомологичного титра.
Изучена чувствительность эпидемических штаммов вирусов гриппа, выделенных в разных городах РФ, к препаратам с антинейраминидазной активностью. Данные представлены в табл. 3.
Таблица 3. Чувствительность эпидемических штаммов вирусов гриппа А и В, выделенных в сезоне 2023–2024 гг., к препаратам с антинейраминидазной активностью
Table 3. The susceptibility of influenza epidemic strains A and B, isolated in season 2023–2024 to inhibitors of neuraminidase
ФБУЗ «Центр гигиены и эпидемиологии» Роспотребнадзора Center for Hygiene and Epidemiology of Rospotrebnadzor | Число штаммов Number of strains | Штаммы вируса гриппа Influenza virus strains | IC50 (nM) к антинейраминидазным препаратам (интервалы среднего значения) IC50 (nM) to antineuraminidase drugs (mean value intervals) | |
осельтамивиру oseltamivir | занамивиру zanamivir | |||
ЦЭЭГ, НИЦЭМ, Москва NRCEM CEEI, Moscow | 2 | A(H1N1)pdm09 | 0,5–0,7 | 0,4–0,9 |
56 | A(H3N2) | 0,3–5,0 | 0,9–8,3 | |
3 | B | 35,6–38,9 | 4,5–5,1 | |
Новгородской области / Novgorod region | 2 | A(H3N2) | 0,9–3,1 | 1,9–4,3 |
Ярославской области / Yaroslavl region | 2 | A(H3N2) | 0,5–0,6 | 0,5–1,6 |
Оренбургской области / Orenburg region | 10 | A(H3N2) | 0,3–0,9 | 0,6–4,2 |
Томской области / Tomsk region | 5 | A(H3N2) | 0,4–0,6 | 0,9–1,2 |
Приморского края / Primorsky Krai | 10 | A(H3N2) | 0,4–0,7 | 0,8–2,0 |
4 | B | 22,0–42,7 | 2,0–7,3 | |
Еврейской АО / Jewish Autonomous District | 4 | A(H3N2) | 0,4–1,0 | 0,8–4,1 |
ИТОГО TOTAL | 2 | A(H1N1)pdm09 | 0,5–0,7 | 0,4–0,9 |
89 | A(H3N2) | 0,3–5,0 | 0,5–8,3 | |
7 | В | 22,0–42,7 | 2,0–7,3 | |
Все из протестированных штаммов проявили нормальную чувствительность к осельтамивиру и занамивиру, за исключением 2 штаммов вируса гриппа A(H3N2) – А/Москва/26/2023 и А/Москва/3/2024 (H3N2), в отношении которых обнаружена сниженная чувствительность к осельтамивиру и занамивиру.
Методом высокопроизводительного секвенирования получены полногеномные последовательности для 62 штаммов вирусов гриппа А, в том числе 58 штаммов A(H3N2) и 4 штаммов A(H1N1)pdm09, выделенных в разных регионах РФ.
Вирусы гриппа A(H3N2) были отнесены к клайду 3C.2a1b.2a.2a.3a.1 (2a.3a.1), представленному вирусом A/Таиланд/8/2022. В отношении 72,0% популяции выявлены общие замены N122D, K276E, характерные для субклайда J.2 (референс-штамм A/Сидней/878/2023); кроме того, были выявлено 12 штаммов, которые так же несли дополнительные мутации в HA, как I25V, V347M, что больше характерно для субклайда J.1 (референс-штамм A/Сидней/856/2023); на Дальнем Востоке были выявлены оригинальные штаммы (13), несущие дополнительные замены F79L, P239S в HA по отношению к клайду J.2: (EPI_ISL_18807375, EPI_ISL_18808360, EPI_ISL_18808361, EPI_ISL_18808362, EPI_ISL_18808363, EPI_ISL_18808364, EPI_ISL_18808365, EPI_ISL_18808371, EPI_ISL_19072582, EPI_ISL_19072580, EPI_ISL_19072579, EPI_ISL_19072578, EPI_ISL_19072577, EPI_ISL_19072576, EPI_ISL_19072575, EPI_ISL_19072574, EPI_ISL_19072573, EPI_ISL_19072572, EPI_ISL_19072571, EPI_ISL_19072570, EPI_ISL_19072569, EPI_ISL_19072524, EPI_ISL_19072523, EPI_ISL_19072522, EPI_ISL_19072521, EPI_ISL_19072520, EPI_ISL_19072519, EPI_ISL_19072518, EPI_ISL_19072517, EPI_ISL_19072516, EPI_ISL_19072515, EPI_ISL_19072514, EPI_ISL_19072513, EPI_ISL_19072512, EPI_ISL_19072511, EPI_ISL_19072510, EPI_ISL_19072509, EPI_ISL_19072508, EPI_ISL_19072507, EPI_ISL_19072506, EPI_ISL_19072505, EPI_ISL_19072504, EPI_ISL_19072503, EPI_ISL_19072502, EPI_ISL_19072501, EPI_ISL_19072500, EPI_ISL_19072499, EPI_ISL_19072498, EPI_ISL_19072497, EPI_ISL_19072496, EPI_ISL_19072495, EPI_ISL_19072494, EPI_ISL_19072493, EPI_ISL_19072492, EPI_ISL_19072491, EPI_ISL_19072490, EPI_ISL_19072489, EPI_ISL_19072488).
Штаммы вируса гриппа A(H1N1)pdm09 (4) были близкородственны вакцинному вирусу А/Виктория/2570/19, представленному клайдом 6B.1A.5a.2a (EPI_ISL_18809332, EPI_ISL_18809333, EPI_ISL_18809334, EPI_ISL_18809335).
Среди изученных штаммов генетических маркеров, ответственных за снижение чувствительности к ингибиторам нейраминидазы (осельтамивира, занамивира) и полимеразного комплекса (балоксавира марбоксила), не выявлено.
Обсуждение
Ранний рост активности вирусов гриппа на фоне относительно низкой активности и продолжающейся эволюционной изменчивости SARS-CoV-2 был отмечен в рассматриваемый период в большинстве стран Северного полушария4,5,6.
По данным ВОЗ, с 1 октября 2023 г. по 30 июня 2024 г. во всех странах мира было проведено исследование более 10 млн образцов клинических материалов, из которых 12,3% оказались положительными на вирусы гриппа. Увеличение показателя выявления положительных проб на вирусы гриппа было отмечено с начала октября 2023 г., с превышением 10% порогового значения в период 47-й недели 2023 г. (11,0%); максимальные показатели были зарегистрированы в период последней недели 2023 г. (33,0%); уменьшение этого показателя началось с 14-й недели 2024 г.; к концу сезона (39-я неделя 2024 г.) он составил 4,0%, что было выше по сравнению с предыдущим сезоном (1,4%). За анализируемый период долевое участие вирусов гриппа распределилось следующим образом: грипп типа А – 78,0% и грипп типа В – 22,0%; 25,0% среди субтипированных вирусов гриппа А были отнесены к A(H1N1)pdm09 и 75,0% – к A(H3N2); все из субтипированных вирусов гриппа В были отнесены к линии В/Виктория-подобных. Прослежены, как и в предыдущие сезоны, различия по долевому участию вирусов гриппа в странах, температурных зонах и регионах ВОЗ.
В странах Европейского региона ВОЗ рост показателей числа положительных проб на респираторные патогены был связан с вирусом гриппа A(H3N2) с максимальными значениями на 5-й неделе 2024 г. (26,1%); снижением в период 9-й недели 2024 г. (9,8%)5. Вирус гриппа В детектировали с 13-й недели 2024 г., в основном в спорадических случаях. За анализируемый период долевое участие распределилось следующим образом: грипп типа А – 43741 (93,4%) и грипп типа В – 3066 (6,4%); 10,4% среди субтипированных вирусов гриппа А пришлось на A(H1N1)pdm09 и 89,6% – на A(H3N2); все из субтипированных вирусов гриппа В (159) были отнесены к линии В/Виктория-подобных.
В странах Американского региона ВОЗ длительность эпидемии гриппа составила 15 нед (с 49-й недели 2023 г.) с максимальными показателями активности в конце декабря 2023 г. (18,1%), при этом были отмечены различия по доминирующему типу вируса: в странах Северной Америки доминировал вирус гриппа типа A(H1N1)pdm09 (76,5% из числа типированных штаммов вируса гриппа А)6; в Центральной Америке и на Карибских островах доминировал A(H3N2) с частотой положительных проб до 81,0%.
В странах Юго-Восточного региона ВОЗ регистрировали относительно низкую активность вирусов гриппа (до 10,0% положительных проб из числа тестируемых), причем детектировали практически равнозначную активность всех 3 вирусов гриппа.
В странах Западного Тихоокеанского региона ВОЗ прослежена большая активность A(H3N2) с пиковыми показателями числа положительных проб на 49-й неделе (34,1%); с 10-й недели 2024 г. регистрировали рост активности вируса гриппа A(H1N1)pdm09 с максимальными показателями в период 13-й недели 2024 г.
В странах Африканского региона ВОЗ с 40-й недели 2023 г. регистрировали со-циркуляцию вирусов гриппа А, причем большую активность A(H1N1)pdm09 отмечали в период некоторых недель сезона, при этом вирус гриппа В выявляли только в спорадических случаях. Показатели, превышающие пороговый уровень (10,0%), регистрировали в период с 40-й недели 2023 г. до 3-й недели 2024 г. и с 18-й до 26-й недели 2024 г. (до 250 положительных проб в неделю). В странах центральной Африки долевое участие вирусов гриппа составило: для гриппа А – 62,0% с равнозначным участием обеих подтипов; гриппа В – 38,0%. В странах восточной Африки долевое участие вирусов гриппа составило: для гриппа А – 87,0%, в том числе гриппа A(H3N2) – 72,0%; гриппа В – 13,0%.
В странах Восточного Средиземноморского региона ВОЗ начало сезона было отмечено относительно высокими показателями числа положительных проб на вирусы гриппа (22,7% в период 40-й недели 2023 г.) с максимальными показателями к 43-й неделе 2023 г. (29,1%). В этот период в ряде стран была отмечена большая активность вирусов гриппа A(H1N1)pdm09 и В – в Бахрейне, Египте и Ливане; социркуляцию A(H3N2) и В регистрировали в Афганистане; A(H1N1)pdm09 и A(H3N2) – в Тунисе.
Изучение генетических свойств популяции циркулировавших штаммов выявило неполное соответствие штаммам, входившим в состав гриппозных вакцин в сезоне 2023–2024 гг., для стран Северного полушария.
Популяция циркулировавших штаммов вируса гриппа A(H1N1)pdm09 была представлена вариантами клайда 5a.2a (субклайдов – С.1, С.7, С.1.7.2, С.8. С.1.9) и клайда 5а.2а.1 (субклайдов С.1.1, D, D.1, D.2, D.3, D.4), включающих эталоны – А/Виктория/2570/2017 (вакцинный), А/Сидней/5/2021, А/Висконсин/67/2022. Наибольшая активность была отмечена в отношении субклайда С.1.9, который доминировал в большинстве регионов, за исключением стран Северной Америки, Центральной и Южной Америки, где доминировали штаммы субклайда D.
Штаммы вируса гриппа A(H3N2) были отнесены к клайду 3C.2a1b.2a.2a.3a.1 (субклайды J.1–J.4; А/Таиланд/18/2022) с доминированием субклайда J.2., представители которого имели специфические замены в гемагглютинине (HA) – N122D и R276E. Штаммы субклайда J.1 (I25V, V347M) социркулировали с небольшой частотой во многих странах, за исключением стран Азии и Африки, где было отмечено их доминирование. В ряде стран западной Африки выявляли циркуляцию субклайдов G.1.3.1 (2a.3a) и J.4 (2a.3a.1).
Вирусы гриппа В были менее активны, и все из типированных вирусов принадлежали к линии В/Виктория-подобных, клайду V1A.3а.2 (В/Австрия/1359417/2021); представители линии В/Ямагата-подобных детектированы не были.
Учитывая особенности свойств циркулировавших штаммов, эксперты ВОЗ провели замену состава гриппозных вакцин компонента вируса гриппа A(H3N2): А/Дарвин/9/2021 (клайд 2а) на A/Таиланд/8/2022 (клайд 2а.3а.1, субклайд J). Необходимо отметить, что в период февраля–сентября 2024 г. в популяции штаммов вирусов гриппа продолжали регистрировать гетерогенность популяций и в большей степени это коснулось вируса гриппа A(H3N2) (доминирующего в России и странах Европы), что стало причиной его замены в составе гриппозных вакцин для стран Южного полушария на более актуальный (A/Таиланд/8/2022, клайд 2а.3а.1, субклайд J на А/Хорватия/10136RV/2023, клайд).
Согласно данным, полученным ВОЗ в период сезона 2023–2024 гг., была протестирована чувствительность более 15 000 штаммов вирусов гриппа А и В к препаратам с антинейраминидазной активностью и около 10 000 – к балоксавирусу марбоксилу. Результаты показали хороший профиль чувствительности ко всем препаратам; в целом пониженная чувствительность к препаратам с антинейраминидазной активностью была определена среди штаммов A(H1N1)pdm09 в 1,6%, A(H3N2) в 0,01% и гриппа В в 0,2%; к балоксавиру марбоксилу в 0,1, 0,3 и 0% соответственно.
Второй респираторный патоген, в отношении которого страны проводят международный мониторинг, – новый коронавирус SARS-CoV-21. В рассматриваемом эпидемическом сезоне его активность была значительно ниже по сравнению с предыдущими сезонами (в основном частота положительных проб не превышала 10,0%, за исключением летних месяцев, в период которых регистрировали максимальные показатели ‒ до 13,0%), при этом его наибольшая активность была отмечена в странах Европейского региона ВОЗ. Суммарно к 15 сентября 2024 г. в мире было зарегистрировано 776 301 484 случая инфицирования SARS-CoV-2, 7 066 329 (0,9%) из которых – с летальным исходом. Тройку лидеров по числу инфицированных составили страны Европы (36,0%), Тихоокеанского региона (27,0%) и Америки (25,0%). В то же время тройку лидеров по частоте летальных исходов составили страны Европы (32,0%), Америки (43,0%) и Юго-Восточной Азии (11,0%). Прослежена зависимость активности SARS-CoV-2 от активности вирусов гриппа; складывается впечатление, что в отличие от предыдущих лет на фоне высокой активности вирусов гриппа снижается активность SARS-CoV-2. Можно предположить, что SARS-CoV-2 «занял свою нишу» в структуре классических ОРВИ.
Кроме того, в популяции этого вируса также были отмечены новые варианты с доминированием в определенные периоды. В начале сезона (октябрь 2023 г.) наиболее часто детектировали варианты XBB 1,5+F456 (64,5%), BA.2 (20,0%) и BA.2.75 (8,0%). В последующие месяцы был отмечен рост варианта BA.2.86 (c ноября 2023 г.), и уже к январю 2024 г. его долевое участие составило 92,0%. Далее в циркуляцию вошли новые варианты по линии BA.2.86, в частности JN.1, изменчивость которого регистрировали в последующие месяцы. JN.1 стал «родоначальником» популяции штаммов, получившей название FLiRT. В период сентября 2024 г. среди наиболее распространенных субклайдов FLiRT в Европейском регионе стали такие представители, как KP.3.1.1 (45%), XEC (13%), KP.3.1 (11%), JN.1 (9%), JN.1.11 (3%), JN.1.16 (3%), JN.1.9 (3%), KP.2 (3%)5.
А.А. Соминина и соавт. сообщили об изменениях в этиологической структуры средней и тяжелой форм ОРВИ в период пандемии COVID-19, в частности, значительном снижении частоты детекции вирусов гриппа и HRsV (2020–2021 гг.), росте числа случаев HMPV- и HRV-инфекций; росте удельного веса HRsV-инфекции у детей на фоне достоверного снижения частоты COVID-19 (2022–2023 гг.) [3]. В отделениях реанимации и интенсивной терапии у детей в постпандемический период чаще всего выявляли HRsV-инфекцию, у взрослых – SARS-CoV-2. Полученные в рамках настоящей работы данные в определенной степени подтверждают выявленные ранее тенденции.
Особую обеспокоенность продолжает вызывать способность вирусов гриппа птиц и свиней инфицировать людей, что нередко приводит к тяжелым случаям заболевания7 [10]. Среди наиболее патогенных – вирусы гриппа А с подтипом гемагглютинина H5, H7 и H9.
В период сентября 2023 г. – августа 2024 г. в некоторых странах мира инфицирование вирусом гриппа птиц A(H5N1) было подтверждено в 23 случаях (Камбоджа – 14, США – 6, по 1 случаю в Китае, Австралии и Вьетнаме), A(H5N6) – 5 случаев (Китай), A(H9N2) – 14 случаев (Китай – 11, по 1 случаю в Гане, Индии и Вьетнаме), A(H10N3) – 1 случай (Китай), A(H10N5) – 1 случай (Китай); инфицирование вирусами гриппа свиней A(H1N1)v – 5 случаев (США, Вьетнам, Бразилия, Испания, Швейцария, A(H1N2 v – 5 случаев (США – 4, Великобритания – 1), A(H3N2)v – 1 случай (Канада)8.
С 2024 г. в США регистрируют случаи инфицирования фермеров вирусом гриппа птиц A(H5N1) от коров (клайд 2.3.4.4.b, генотип B3.13) и от птиц на птицефабриках (генотипа D1.1)6. При этом случаев передачи от человека к человеку не регистрировали с 2007 г. Возможно, это коррелирует с данными в опытах на хорьках, где было показано, что вирус клайда 2.3.4.4.b, включая генотип B3.13, достаточно хорошо передавался при прямом контакте и крайне ограниченно – при воздушно-капельном [11]. Современные вирусологические и эпидемиологические данные показывают, что несмотря на способность вирусов гриппа птиц инфицировать людей, по своим свойствам они остаются птичьими без «признаков» адаптации к млекопитающим, хотя события 2024 г. в США утверждают обратное: вирус гриппа птиц A(H5N1) смог инфицировать коров, а от коров произошло инфицирование людей. Все вышесказанное определяет необходимость дальнейших исследований и контроля.
Заключение
Эпидемический сезон 2023–2024 гг. имел свои особенности и, в частности, на фоне относительно низкой активности SARS-CoV-2 и его новых вариантов характеризовался более ранним началом, наибольшей активностью вируса гриппа А, причем страны мира различались по доминирующему подтипу (A(H1N)pdm09 или A(H3N2)), а также долевому участию вируса гриппа В линии В/Виктория-подобных; вирус гриппа линии В/Ямагата-подобных не проявлял свою активность с марта 2020 г. В зависимости от активности типа/подтипа вируса гриппа в определенные периоды сезона отмечены различия по показателям заболеваемости, вовлеченности возрастных групп, летальности. По антигенным и молекулярно-генетическим свойствам популяция эпидемических штаммов вирусов гриппа была близка вирусам, входившим в состав гриппозных вакцин, рекомендованных экспертами ВОЗ в сезоне 2022–2023 гг., что предполагает их высокую эффективность; сохранен благоприятный профиль чувствительности к препаратам с антинейраминидазной активностью, а также ингибитору фермента, синтезирующего матричную РНК вируса гриппа. Тройку «лидеров» в структуре сезонных ОРВИ представляли HRV (5,9%), HRsV (2,4%) и HCoV (2,1%). В странах мира продолжают регистрировать случаи инфицирования людей вирусами гриппа птиц и свиней. Все вышесказанное указывает на актуальность исследований и полученных данных в рамках проводимого надзора за циркуляцией вирусов гриппа.
1 COVID-19 epidemiological update – 9 October 2024. Edition 172. Доступно по: https://www.who.int/publications/m/item/covid-19-epidemiological-update-edition-172
2 Risk assessments and summaries of influenza at the human-animal interface. Доступно по: https://www.who.int/teams/global-influen-za-programme/avian-influenza/monthly-risk-assessment-summary
3 Опубликованы рекомендации по штаммовому составу вакцин против сезонного гриппа на 2024–2025 гг. для Северного полушария; 2024. Доступно по: https://www.who.int/ru/news/item/23-02-2024-recommendations-announced-for-influenza-vaccine-composition-for-the-2024-2025-northern-hemisphere-influenza-season
4 Global influenza programme. Influenza updates. Доступно по: https://www.who.int/teams/global-influenza-programme/surveillance-and-monitoring/influenza-updates
5 Seasonal influenza – Annual Epidemiological Report for 2023/2024. Доступно по: https://www.ecdc.europa.eu/en/publications-data/seasonal-influenza-annual-epidemiological-report-20232024
6 Seasonal influenza – Annual Epidemiological Report for 2023/2024. Доступно по: https://www.ecdc.europa.eu/en/publications-data/seasonal-influenza-annual-epidemiological-report-20232024
7 Опубликованы рекомендации по штаммовому составу вакцин против гриппа на эпидемический сезон 2025 г. в Южном полушарии; 2024. Доступно по: https://www.who.int/ru/news/item/27-09-2024-recommendations-announced-for-influenza-vaccine-composition-for-the-2025-southern-hemisphere-influenza-season
8 Influenza (avian and other zoonotic). Доступно по: https://www.who.int/health-topics/influenza-avian-and-other-zoonotic#tab=tab_1
Об авторах
Елена Ивановна Бурцева
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Автор, ответственный за переписку.
Email: elena-burtseva@yandex.ru
ORCID iD: 0000-0003-2518-6801
д-р мед. наук, заведующая лабораторией этиологии и эпидемиологии гриппа
Россия, 123098, г. МоскваНаталья Владимировна Бреслав
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: n.belyakova1983@gmail.com
ORCID iD: 0000-0002-6946-5119
канд. биол. наук, старший научный сотрудник
Россия, 123098, г. МоскваЕвгения Андреевна Мукашева
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: mukasheva_evgeniya@mail.ru
ORCID iD: 0000-0002-5688-5309
научный сотрудник
Россия, 123098, г. МоскваКирилл Геннадьевич Краснослободцев
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: kkg_87@mail.ru
ORCID iD: 0000-0003-1745-9128
научный сотрудник
Россия, 123098, г. МоскваЕлена Сергеевна Кириллова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: esshevchenko@yandex.ru
ORCID iD: 0000-0001-7977-7530
канд. мед. наук, ведущий научный сотрудник
Россия, 123098, г. МоскваСветлана Викторовна Трушакова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: s.trushakova@gmail.com
ORCID iD: 0000-0002-9610-3041
канд. биол. наук, старший научный сотрудник
Россия, 123098, г. МоскваИрина Александровна Комарова
ФГБОУ ВО «Тихоокеанский государственный медицинский университет» Минздрава России
Email: mikhaira@yandex.ru
ORCID iD: 0000-0003-0483-7433
ассистент кафедры инфекционных болезней
Россия, 690002, г. ВладивостокЕлена Леонидовна Феодоритова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: flulab@mail.ru
ORCID iD: 0000-0002-1472-1357
научный сотрудник
Россия, 123098, г. МоскваАнна Дмитриевна Панова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: ainushgnomello@gmail.com
ORCID iD: 0000-0002-9322-6273
младший научный сотрудник
Россия, 123098, г. МоскваЛидия Борисовна Кистенева
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: lborisovna2007@yandex.ru
ORCID iD: 0000-0001-7336-409X
руководитель лаборатории
Россия, 123098, г. МоскваИрина Николаевна Хлопова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: khlopova.ira@yandex.ru
ORCID iD: 0000-0002-7419-590X
канд. мед. наук, ведущий научный сотрудник Института вирусологии им. Д.И. Ивановского
Россия, 123098, г. МоскваИрина Сергеевна Кружкова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: irina-kru@yandex.ru
ORCID iD: 0000-0002-1983-481X
младший научный сотрудник
Россия, 123098, г. МоскваАнастасия Сергеевна Крепкая
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: nastya18-96@mail.ru
ORCID iD: 0000-0002-7272-4011
младший научный сотрудник
Россия, 123098, г. МоскваЕкатерина Олеговна Морозова
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: eo-morozova@inbox.ru
ORCID iD: 0009-0001-3367-6168
канд. биол. наук, старший научный сотрудник
Россия, 123098, г. МоскваАнна Викторовна Игнатьева
ФГБУ «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Минздрава России
Email: valgella@yandex.ru
ORCID iD: 0000-0001-6206-2299
канд. биол. наук, старший научный сотрудник
Россия, 123098, г. МоскваАндрей Борисович Комиссаров
ФГБУ «Научно-исследовательский институт гриппа им. А.А. Смородинцева» Минздрава России
Email: andrey.komissarov@influenza.spb.ru
ORCID iD: 0000-0003-1733-1255
заведующий лабораторией молекулярной вирусологии
Россия, 197022, г. Санкт-ПетербургИгорь Николаевич Тюрин
ГБУЗ «Инфекционная клиническая больница № 1» Департамента здравоохранения города Москвы
Email: tyurin.dti@yandex.ru
ORCID iD: 0000-0002-5696-1586
канд. мед. наук, главный врач
Россия, 125310, г. МоскваАлексей Александрович Самков
ГБУЗ «Инфекционная клиническая больница № 1» Департамента здравоохранения города Москвы
Email: a.a.samkov@yandex.ru
ORCID iD: 0000-0002-0365-3096
заместитель главного врача по медицинской части
Россия, 125310, г. МоскваНаталья Александровна Антипят
ГБУЗ «Инфекционная клиническая больница № 1» Департамента здравоохранения города Москвы
Email: natadoc70@bk.ru
ORCID iD: 0000-0001-8578-2838
заместитель главного врача по медицинской части
Россия, 125310, г. МоскваСписок литературы
- Бурцева Е.И., Колобухина Л.В., Воронина О.Л., Игнатьева А.В., Мукашева Е.А., Панова А.Д. и др. Особенности циркуляции возбудителей ОРВИ на фоне появления и широкого распространения SARS-CoV-2 в 2018–2021 годы. Эпидемиология и Вакцинопрофилактика. 2022; 21(4): 16–26. https://doi.org/10.31631/2073-3046-2022-21-4-16-26 https://elibrary.ru/rnyfoi
- Бурцева Е.И., Колобухина Л.В., Панова А.Д., Мукашева Е.А., Краснослободцев К.Г., Кириллова Е.С. и др. Свойства вирусов гриппа, вызвавших эпидемические подъемы заболеваемости в России и странах мира в 2022–2023 гг. Эффективность вакцинопрофилактики. Вопросы вирусологии. 2024; 69(1): 42–55. https://doi.org/10.36233/0507-4088-211 https://elibrary.ru/zqtfnx
- Соминина А.А., Даниленко Д.М., Комиссаров А.Б., Писарева М.М., Мусаева Т.Д., Столяров К.А. и др. Изменения этиологической структуры тяжёлых острых респираторных вирусных инфекций у детей и взрослых под влиянием пандемии СOVID-19. Журнал микробиологии, эпидемиологии и иммунобиологии. 2024; 101(3): 327–41. https://doi.org/10.36233/0372-9311-532 https://elibrary.ru/jmtwkj
- Петрова П.А., Коновалова Н.И., Бояринцева А.Ю., Даниленко Д.М., Васильева А.Д., Шелепанова Т.Н. и др. Этиологическая характеристика эпидемий гриппа на территории России в период пандемии COVID-19 в 2020–2023 гг. Эпидемиология и Вакцинопрофилактика. 2024; 23(3): 88–97. https://doi.org/10.31631/2073-3046-2024-23-3-88-97 https://elibrary.ru/ofrzhj
- Карпова Л.С., Пелих М.Ю., Поповцева Н.М., Столярова Т.П., Волик К.М., Столяров К.А. Коронавирусная инфекция, вызванная вариантом «омикрон» и его дочерними геновариантами в России (2022–2023 гг.). Эпидемиология и Вакцинопрофилактика. 2024; 23(2): 36–49. https://doi.org/10.31631/2073-3046-2024-23-2-36-49 https://elibrary.ru/uqdnmi
- Карпова Л.С., Комиссаров А.Б., Столяров К.А., Поповцева Н.М., Столярова Т.П., Пелих М.Ю. и др. Особенности эпидемического процесса COVID-19 в каждую из пяти волн заболеваемости в России. Эпидемиология и Вакцинопрофилактика. 2023; 22(2): 23–36. https://doi.org/10.31631/2073-3046-2023-22-2-23-36 https://elibrary.ru/udxfrp
- Пшеничная Н.Ю., ред. Грипп и ОРВИ в XXI веке: руководство для врачей. М.: ГЭОТАР-Медиа; 2024. https://doi.org/10.33029/9704-8433-3-IAR-2024-1-304
- Zhou B., Lin X., Wang W., Halpin R.A., Bera J., Stockwell T.B., et al. Universal influenza B virus genomic amplification facilitates, sequencing, diagnostics, and reverse genetics. J. Clin. Microbiol. 2014; 52(5): 1330–7. https://doi.org/10.1128/jcm.03265-13
- Zhou B., Donnelly M.E., Scholes D.T., St George K., Hatta M., Kawaoka Y., et al. Single-reaction genomic amplification accelerates sequencing and vaccine production for classical and swine origin human influenza A viruses. J. Virol. Oct. 2009; 83(19): 10309–13. https://doi.org/10.1128/jvi.01109-09
- Charostad J., Rezaei Zadeh Rukerd M., Mahmoudvand S., Bashash D., Hashemi S.M.A., Nakhaie M., et al. A comprehensive review of highly pathogenic avian influenza (HPAI) H5N1: An imminent threat at doorstep. Travel Med. Infect. Dis. 2023; 55: 102638. https://doi.org/10.1016/j.tmaid.2023.102638
- Belser J.A., Sun X., Pulit-Penaloza J.A., Maines T.R. Fatal infection in ferrets after ocular inoculation with highly pathogenic avian influenza A(H5N1) virus. Emerg. Infect. Dis. 2024; 30(7): 1484–7. https://doi.org/10.3201/eid3007.240520
Дополнительные файлы