Диагностика инфекционного и гемагглютинирующего титра вируса гриппа А/Маллард Пенсильвания/10218/84 (H5N2) по изменению микровязкости вирусной мембраны после взаимодействия с фосфолипидными модификаторами на примере бесхолестериновых липосом
- Авторы: Контаров Н.А.1,2, Погарская И.В.2, Долгова Е.И.2, Контарова Е.О.3, Помазанов В.В.4, Гафаров Р.Р.4, Марданлы С.Г.4, Юминова Н.В.2
-
Учреждения:
- ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет)
- ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова»
- ФГБУ «Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий» ФМБА России
- ГОУ ВО МО «Государственный гуманитарно-технологический университет»
- Выпуск: Том 70, № 5 (2025)
- Страницы: 471-476
- Раздел: В ПОМОЩЬ ВИРУСОЛОГУ
- URL: https://virusjour.crie.ru/jour/article/view/16798
- DOI: https://doi.org/10.36233/0507-4088-326
- EDN: https://elibrary.ru/atftvd
- ID: 16798
Цитировать
Полный текст
Аннотация
Введение. Противовирусное действие ряда препаратов связано с модификацией липидной мембраны вирусов вследствие их применения. Один из возможных механизмов такой модификации вирусной мембраны заключается в экстракции холестерина из мембран вирионов.
Цель работы. Изучить методику определения инфекционного и гемагглютинирующего титра вируса гриппа птиц по изменению микровязкости вирусной мембраны после инкубации с фосфолипидными модификаторами ‒ бесхолестериновыми липосомами, состоящими из фосфатидилхолина и фосфатидилэтаноламина в мольном отношении 1 : 2, в течение 48 ч.
Материалы и методы. Процесс экстракции подтверждали двумя методами: гель-фильтрацией с радиоактивно меченными липосомами и вирионами, а также по изменению величины поляризации флуоресцентного зонда 1-анилинонафталин-8-сульфонат-аниона (8-АНС) в вирусной мембране.
Результаты. Обнаружена корреляционная связь между изменением инфекционного и гемагглютинирующего титра и микровязкостью вирусной мембраны.
Заключение. Предложенная в работе методика позволяет проводить количественное определение инфекционной и гемагглютинирующей активности вируса гриппа в зависимости от изменений микровязкости мембран вирусов после взаимодействия фосфолипидных модификаторов. Представляется возможным использовать выявленную зависимость для определения инфекционной и гемагглютинирующей активности вируса гриппа в пределах одного серотипа в клинической лабораторной диагностике, применяя различные флуоресцентные зонды. В качестве липофильных модификаторов вирусной мембраны можно использовать не только липосомы определенного состава, но и такие соединения, как этиленгликоль, эритрит, глицерин.
Полный текст
Введение
На сегодняшний день имеется значительное количество работ, посвященных изучению противовирусного действия липосом в комплексе с разными химическими соединениями и методам изучения механизмов взаимодействия таких липосом с разными оболочечными вирусами [1–9]. Обмен липидами с липосомами приводит к изменению физических характеристик локального окружения белковых антигенов вируса гриппа и к невозможности изменения их конформации при взаимодействии с рецепторами клетки-хозяина. При этом в литературе отсутствует информация о наличии зависимости между величинами инфекционного и гемагглютинирующего титра вируса гриппа от физических характеристик вирусной мембраны. Одной из таких характеристик, которую достаточно просто определить, используя различные флуоресцентные зонды, является микровязкость, что может являться диагностическим признаком. Изменение микровязкости зависит от содержания холестерина в мембране.
Цель – разработать метод, позволяющий определять инфекционный и гемагглютинирующий титр вируса гриппа в зависимости от изменения микровязкости вирусной мембраны после взаимодействия с бесхолестериновыми липосомами.
Материалы и методы
Объектом исследования служил штамм вируса гриппа птиц А/Маллард Пенсильвания/10218/84 (H5N2). Вирус выращивали на 10-дневных куриных эмбрионах. Исходный инфекционный титр вируса составлял 7,0 ± 0,2 lg 50% эмбриональных инфицирующих доз в 1 мл (ЭИД50/мл). Изучение противовирусного действия вируса проводили в перевиваемой культуре клеток MDCK (клетки почек собаки Мадина–Дарби). Клетки линии MDCK высевали на 24-луночные планшеты и инкубировали 14–24 ч до формирования монослоя, занимающего от 80 до 90% ростовой поверхности. Затем вносили в лунки по 0,1 мл вируссодержащей жидкости (множественность инфекции составляла 0,01 ТЦД50/кл (50% тканевая цитопатическая доза на клетку)) в среде альфа-МЕМ и инкубировали в течение 72 ч в атмосфере СО2 при 36 °С. После инкубации клетки промывали средой МЕМ и вносили бесхолестериновые липосомы в лунки планшетов с монослоем клеток в объеме 0,5 мл. Планшеты с клетками инкубировали в атмосфере СО2 при 36 °С в течение 30 мин. Затем в культуральной жидкости определяли инфекционный и гемагглютинирующий титр вируса. Инфекционность вируса определяли по титрованию в 10-дневных куриных эмбрионах при их заражении в аллантоисную полость. Инфекционный титр рассчитывали по методу Рида–Менча. Реакцию гемагглютинации проводили стандартным образом с использованием куриных эритроцитов [10]. Исходный гемагглютинирующий титр составлял 2048 ГАЕ/мл. Липосомы получали по стандартному методу с незначительными модификациями [11]. Препарат фосфатидилхолина (Sigma, США) в концентрации 1–2 мг/мл в растворе 0,01 М KCl инкубировали при 70 °С в течение 10 мин, также использовали препараты смеси фосфатидилэтаноламина и фосфатидилхолина (Sigma, США) в мольном соотношении 2 : 1. Размеры и частичную концентрацию липосом определяли спектрофотометрически с помощью фотоэлектроколориметра (ФЭК) по методу Геллера [12]. Для стабилизации липосом добавляли полиэтиленгликоль 6000 (Sigma, США) в конечной концентрации 2,5 мМ. Распределение липосом из смеси фосфолипидов по размерам представляло собой гамма-распределение со средним радиусом липосом –R = 85 ± 2,5 нм, средний индекс полидисперности липосомальных дисперсий составлял менее 0,1. Средняя частичная концентрация липосом из смеси фосфолипидов составила ––N = (6,45 ± 0,1) × 1015 см3. Определение степени окисленности липосом проводили по общепринятой методике с расчетом индекса окисленности (ИО):
(1),
где D233, D215 и D300 – оптическая плотность анализируемого образца, измеренная относительно 95% этилового спирта на спектрофотометре Anthos Zenyth 200th (Biochrom, Великобритания) при длинах волн 233, 215 и 300 нм соответственно. Стабильность липосомальной дисперсии оценивали по изменению размеров частиц в зависимости от срока хранения (при температуре 4 °С в течение 20 сут), светопропусканию при длине волны 640 нм с помощью спектрофотометра Anthos Zenyth 200th (Biochrom, Великобритания) и дзета-потенциалу (ζ) который определяли по электрофоретической подвижности липосом в дисперсии методом микроэлектрофореза с помощью прибора Zetasizer-2 (Великобритания). С целью выявления экстракции холестерина липосомами применяли гель-фильтрацию и радиометрию меченных 14С-холестерином вирионов и 3Н-инулином липосом в колонке для гель-фильтрации с сефарозой 4В (Sigma, США). Отсутствие вирионов в фильтрате в обоих случаях контролировали с помощью реакции гемагглютинации [10]. Радиометрию образцов осуществляли с помощью радиометра (БЛ-БДБ-2, РФ). Для определения изменения микровязкости липидной мембраны вирионов и липосом применялся флуоресцентный зонд 8-АНС («Sigma», США) в конечной концентрации 10 мкМ. Для определения величины поляризации (Р) использовали спектрофлюориметр Флюорат-02-Панорама (РФ), λвозб = 360 нм, λэмис = 400–550 нм. Величину Р определяли по формуле Перрена–Яблонского:
(2),
где Р – поляризация флуоресценции зонда в мембране; V – молярный объем зонда, τ0 – время жизни флуоресценции, Р0 – предельная поляризация флуоресценции зонда, η – вязкость среды, R – газовая постоянная, T – температура среды, равная 298 К, κ – постоянная Больцмана. Поляризацию флуоресценции зонда в вирусном инокуляте определяли до добавления липосом и после инкубации с липосомами, как описано выше, в течение 48 ч. Контрольный препаратом являлся вирусный инокулят. Количественной оценкой противовирусного действия липосом являлась величина ΔT (lgЭИД50/мл), равная разности инфекционных титров до и после внесения липосом. Статистическую обработку результатов, полученных из 4-кратных повторов каждого эксперимента, проводили стандартными методами с помощью Microsoft Excel 2010 с проверкой выборки на нормальное распределение с помощью критерия Колмогорова и расчета t-критерия, различия считали достоверными при p ≤ 0,05.
Результаты
На первом этапе исследований было проведено изучение стабильности липосомальных дисперсий. На рис. 1 представлена зависимость, отражающая стабильность липосомальных дисперсий в зависимости от срока хранения при 4 °С. На рисунке видно незначительное, в пределах ошибки, увеличение среднего радиуса липосом в дисперсии при хранении. Светопропускание липосомальной дисперсии при температуре 25 °С и длине волны 640 нм составляло 75%, что соответствует требованиям Государственной фармакопеи РФ. Известно, что устойчивость коллоидных растворов наблюдается при значениях дзета-потенциала более 30 мВ по абсолютному значению [13]. Среднее абсолютное значение дзета-потенциала липосом составило ζ = 65 ± 1,5 мВ. Значение ИО исходной дисперсии липосом составило 0,1, при хранении в течение 20 сут при температуре 4 °С ИО незначительно увеличился до 0,15. В обоих случаях ИО не превышал предельного значения, равного 0,4.
Рис. 1. Изменение размеров липосом при 4 °С в течение 20 сут.
Fig. 1. Change in liposome size at 4 °C for 20 days.
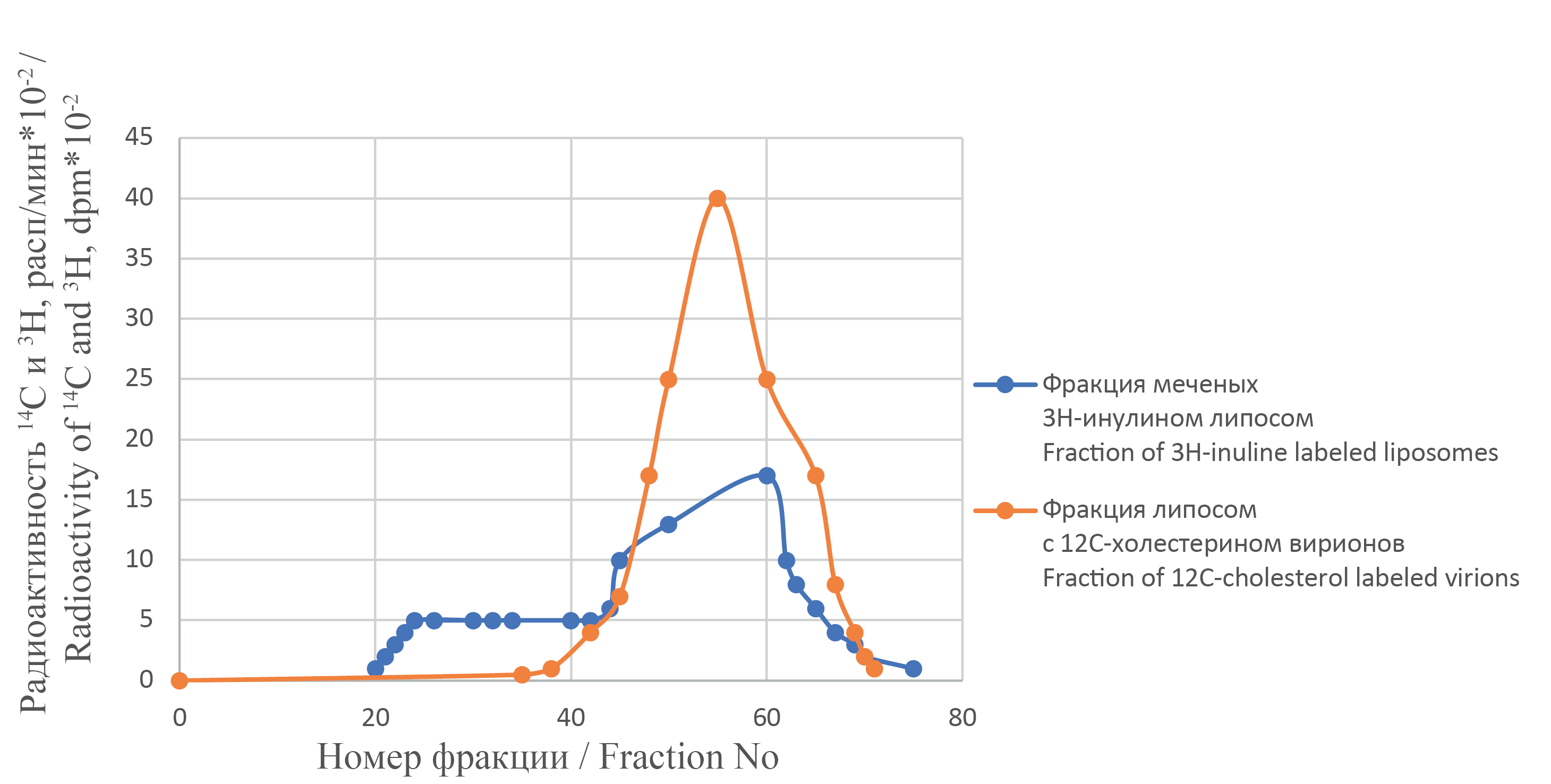
С целью проверить гипотезу экстракции холестерина из вирусной мембраны, после инкубации с вирионами, меченными 14С-холестерином в течение 5 ч, дисперсию с меченными 3Н-инулином липосомами фракционировали по размерам гель-фильтрацией на сефарозе 4В. Было обнаружено, что основная часть меченых липидов находится в составе частиц, совпадающих по своим размерам с исходными липосомами. Совпадали не только средние размеры, но и распределение по размерам. Небольшая фракция липосом в результате взаимодействия с вирионами превратилась в более крупные агрегаты. В их составе также присутствовал вирусный холестерин (рис. 2). Экстракция холестерина из вирионов возможна только при контактном взаимодействии липосом и вирионов. Такая ситуация может наблюдаться при разрушении двойного электрического слоя вирусных мембран липосомами. Экстракция холестерина бесхолестериновыми липосомами приводила к снижению микровязкости вирусных мембран, что было подтверждено с помощью определения величины поляризации флуоресценции зондов по формуле (2). Расчеты показали уменьшение микровязкости вирусных мембран с (5,0 ± 0,4) × 10–3 Па∙с до (1,0 ± 0,05) × 10–3 Па∙с в течение 48 ч после инкубации с липосомами. В вирусном контроле уменьшение микровязкости мембран не происходило. На основании полученных результатов было сделано предположение о возможной корреляции инфекционной и гемагглютинирующей активности вируса от микровязкости мембран вирионов, и, поскольку изменение микровязкости вирусной мембраны вызывает изменение пространственного расположения антигенных белков, последнее может быть использовано в качестве диагностического признака. Были получены зависимости инфекционного и гемагглютинирующего титра от микровязкости вирусных мембран с высоким коэффициентом корреляции. На рис. 3 представлена убывающая линейная зависимость инфекционного титра от микровязкости мембраны вируса. Для гемагглютинирующего титра была получена убывающая экспоненциальная зависимость (рис. 4). На графиках приведены уравнения линий тренда, по которым можно рассчитывать показатели инфекционной и гемагглютинирующей активности по экспериментально определенным значениям микровязкости мембран для конкретного штамма вируса гриппа.
Рис. 2. Гель-фильтрация радиоактивно меченых 3Н-инулином липосом без холестерина и 14С-холестерином вирионов гриппа.
Fig. 2. Gel filtration of radioactively labeled 3H-inulin-free cholesterol-liposomes and 14C-cholesterollabeled influenza virions.
Рис. 3. Зависимость инфекционного титра вируса от микровязкости вирусной мембраны.
Fig. 3. Dependence of infectious titer of the virus on the microviscosity of the viral membrane.
Рис. 4. Зависимость гемагглютинирующего титра вируса от микровязкости вирусной мембраны.
Fig. 4. Dependence of the hemagglutinating titer of the virus on the microviscosity of the viral membrane.
Заключение
Таким образом, предложенная в работе методика позволяет проводить количественное определение инфекционной и гемагглютинирующей активности вируса гриппа в зависимости от изменений микровязкости мембран вирусов после взаимодействия фосфолипидных модификаторов. Данный метод может найти применение в вирусологических исследованиях и клинической лабораторной диагностике при определении инфекционной и гемагглютинирующей активности вирусов гриппа.
Следует отметить, что изменение микровязкости вирусной мембраны может происходить при взаимодействии с любыми другими фосфолипидными модификаторами, которые можно использовать для определения вышеуказанных титров вируса гриппа.
Об авторах
Николай Александрович Контаров
ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» Минздрава России (Сеченовский Университет); ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова»
Автор, ответственный за переписку.
Email: kontarov@mail.ru
ORCID iD: 0000-0003-0030-4867
канд. биол. наук, ведущий научный сотрудник лаборатории детских вирусных инфекций
Россия, 119991, Москва; 115088, МоскваИрина Владимировна Погарская
ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова»
Email: kozyr81@mail.ru
ORCID iD: 0000-0003-3580-6277
канд. биол. наук, ведущий научный сотрудник отдела вирусологии им. О.Г. Анджапаридзе
Россия, 115088, МоскваЕкатерина Игоревна Долгова
ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова»
Email: dolgovaev@mail.ru
ORCID iD: 0000-0001-8985-7569
младший научный сотрудник отдела вирусологии им. О.Г. Анджапаридзе
Россия, 115088, МоскваЕлена Олеговна Контарова
ФГБУ «Федеральный научно-клинический центр специализированных видов медицинской помощи и медицинских технологий» ФМБА России
Email: kontarova@mail.ru
ORCID iD: 0000-0002-5550-7875
канд. мед. наук, врач лучевой диагностики
Россия, 115682, МоскваВладимир Васильевич Помазанов
ГОУ ВО МО «Государственный гуманитарно-технологический университет»
Email: ecolab@mail.ru
ORCID iD: 0000-0002-7336-9912
д-р техн. наук, профессор
Россия, 142611, Орехово-ЗуевоРамис Рафикович Гафаров
ГОУ ВО МО «Государственный гуманитарно-технологический университет»
Email: gafarov68@mail.ru
ORCID iD: 0009-0009-2869-7421
канд. биол. наук
Россия, 142611, Орехово-ЗуевоСейфаддин Гашимович Марданлы
ГОУ ВО МО «Государственный гуманитарно-технологический университет»
Email: ecolab@mail.ru
ORCID iD: 0000-0003-3650-2363
д-р мед. наук
Россия, 142611, Орехово-ЗуевоНадежда Васильевна Юминова
ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова»
Email: yuminova@mail.ru
ORCID iD: 0000-0002-7723-4038
д-р биол. наук, главный научный сотрудник отдела вирусологии им. О.Г. Анджапаридзе
Россия, 115088, МоскваСписок литературы
- Kingery-Wood J.E., Williams K.W., Sigal G.B., Whitesides G.M. The agglutination of erythrocytes by influenza virus is strongly inhibited by liposomes incorporating an analog of sialyl gangliosides. J. Am. Chem. Soc. 1992; 114(18): 7303–5. https://doi.org/10.1021/ja00044a057
- van Meer G., Davoust J., Simons K. Parameters affecting low pH-mediated fusion of liposomes with the plasma membrane of cells infected with influenza virus. Biochemistry. 1985; 24(14): 3593–602. https://doi.org/10.1021/bi00335a030
- Hendricks G.L., Weirich K.L., Viswanathan K., Li J., Shriver Z.H., Ashour J., et al. Sialylneolacto-N-tetraose c (LSTc)-bearing liposomal decoys capture influenza a virus. J. Biol. Chem. 2013; 288(12): 8061–73. https://doi.org/10.1074/jbc.m112.437202
- White J., Helenius A. pH-dependent fusion between the Semliki Forest virus membrane and liposomes. Proc. Natl Acad. Sci. USA. 1980; 77(6): 3273–77. https://doi.org/10.1073/pnas.77.6.3273
- Sulczewski F.B., Liszbinski R.B., Romão P.R.T., Rodrigues Junior L.C. Nanoparticle vaccines against viral infections. Arch. Virol. 2018; 163(9): 2313–25. https://doi.org/10.1007/s00705-018-3856-0
- Hernandez L.D., Peters R.J., Delos S.E., Young J.A., Agard D.A., White J.M. Activation of a retroviral membrane fusion protein: soluble receptor-induced liposome binding of the ALSV envelope glycoprotein. J. Cell Biol. 1997; 139(6): 1455–64. https://doi.org/10.1083/jcb.139.6.1455
- McGill A.R., Markoutsa E., Mayilsamy K., Green R., Sivakumar K., Mohapatra S., et al. Acetate-encapsulated linolenic acid liposomes reduce SARS-CoV-2 and RSV infection. Viruses. 2023; 15(7): 1429. https://doi.org/10.3390/v15071429
- Grünewald K. Viral fusion: how Flu induces dimples on liposomes. EMBO J. 2010; 29(7): 1165-6. https://doi.org/10.1038/emboj.2010.35
- Hendricks G.L., Velazquez L., Pham S., Qaisar N., Delaney J.C., Viswanathan K., et al. Heparin octasaccharide decoy liposomes inhibit replication of multiple viruses. Antiviral Res. 2015; 116: 34–44. https://doi.org/10.1016/j.antiviral.2015.01.008
- Mahy B.W.J. Virology: A Practical Approach. IRL Press; 1985. https://doi.org/10.1136/jcp.38.11.1319-a
- Pagano R., Thompson T.E. Spherical lipid bilayer membranes. Biochim. Biophys. Acta. 1967; 144(3): 666–9. doi: 10.1016/0005-2760(67)90055-0
- Контаров Н.А., Лотте В.Д., Контарова Е.О., Балаев Н.В., Юминова Н.В., Зверев В.В. New method for measurement of size and concentration of lyposomes. Журнал микробиологии, эпидемиологии и иммунобиологии. 2009; 86(6): 95–8. https://elibrary.ru/rcdmzz
- Sabın J., Prieto G., Ruso J.M., Hidalgo-Alvarez R., Sarmiento F. Size and stability of liposomes: A possible role of hydration and osmotic forces. Eur. Phys. J. E. Soft Matter. 2006; 20(4): 401–08. https://doi.org/10.1140/epje/i2006-10029-9
Дополнительные файлы